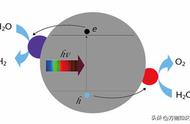
实际上,电化学腐蚀是一种原电池反应,它跟电解池的区别如下:

金属的氧化实际上是一种金属的腐蚀,金属的氧化有狭义和广义两种含义,狭义的含义是指金属与环境介质中的氧化合而生成金属氧化物的过程;广义金属氧化就是金属与介质作用失去电子的过程,对于广义的氧化而言,反应产物不一定是氧化物,也可以是硫化物、卤化物、或其他化合物。本文主要针对狭义的氧化进行介绍。

很多情况下,金属的氧化腐蚀对金属的性能具有破坏性,如铁制品生锈生成Fe2O3,但并非氧化就是无益的,比如,不锈钢不生锈的原因是因为钢中含有铬等合金元素,铬元素极易氧化,当钢中含较多的铬元素时,铬与腐蚀介质中的氧作用,在钢表面形成一层很薄的氧化膜( 自钝化膜),可阻止钢的基体进一步被腐蚀。
同理,铝是一种活泼金属,极易被氧化,在不同的环境条件下,发生不一样的氧化。
自然氧化
铝合金型材在自然环境下会和空气中的氧气发生反应,表面形成一层氧化铝保护层,阻止了内部基体与氧气继续发生反应。而这层保护层是透明的,我们称之为氧化膜。这层氧化膜非常薄,一般说来在0.005-0.015um的范围内。然而这个厚度范围耐腐蚀性不强,不足以保护铝合金型材免遭腐蚀,也不足以作为有机涂层的可靠底层,无法在工业上进行应用。
化学氧化
铝及铝合金化学氧化是指在不通电的条件下,铝及铝合金在适当的温度范围内浸入氧化溶液中发生化学反应,在其表面生成与基体有一定结合力的、不溶性的氧化膜的工艺。在反应过程中,溶解在溶液中的三价铝离子(Al3 )与溶液中的氧化剂、氢氧根(OH-)结合生成三氧化二铝(Al2O3)和氢氧化铝[Al(OH)3]。这种由Al2O3和Al(OH)3组成的氧化膜厚度比自然氧化膜增加了100—200倍,厚度约为0.5~4微米,且多孔,具有良好的吸附性,可作为有机涂层的底层。
但由于膜层没有疏松的孔隙,阻碍了溶液与基体的接触,使得膜层生长停止,膜的厚度不够厚,且质软,其耐磨性和抗蚀性能均不如阳极氧化膜;所以,除有特殊用途外,很少单独使用.但它有较好的吸附能力,在其表面再涂漆,可有效地提高铝制品的耐蚀性和装饰性。
化学氧化通常也叫导电氧化,氧化铝本身不导电,但化学氧化膜还是很薄的,致密性不够,且不均匀,氧化膜因为厚度小并不能提供很大的电阻,起不到绝缘性的作用。所以如果对材料有导电的要求,又要防腐蚀的话可以采用化学氧化。
阳极氧化
一、为什么铝合金要做阳极氧化加工:主要是为了扩大铝的应用范围和使用寿命。我们知道,铝或铝合金优点非常多,如密度小、比强度高、加工性能好、热传导性高、导电好等等。但铝合金本身缺点与弱点同样也非常多:
1.硬度比较低,与此同时耐磨性也比较差。
2.凝固时体积收缩大。
3.膨胀系数高。
4.熔点比较低,使用温度不能超过200℃,因此高温使用受限制。
5.弹性模量只有钢的1/3。
6.电位很负,因此铝与异种金属接触时,容易作为阳极产生严重的电偶腐蚀。
铝没法像钢材那样通过热处理的方法来提高其力学性能和表面性能,虽然通过合金化可提高铝的强度,但其表面性能基本没有提高,从而限制其作为外观零件的应用。
为了克服铝和铝合金的上述缺点(主要是铝表面性能的缺点),从而扩大铝的应用范围和使用寿命。通过对铝和铝合金进行阳极氧化可以做到这一点。
阳极氧化,是将铝或铝合金等金属置入酸性电解质溶液中,作为阳极,通高压直流电,使阴离子向阳极移动,并在阳极产生新生氧与阳极的铝合金生成氧化膜的过程,由于阳极氧化需要在通电的条件下进行,因此也叫电化学氧化。
阳极氧化的目的,从根本上说就是在铝及其合金表面形成一层氧化膜,提高铝及其合金的防护性、装饰性和功能性,扩大其应用范围和使用寿命。
二、阳极氧化膜的性质(与化学氧化膜相比)
氧化膜的主要成分是氧化铝(Al2O3),氧化铝是一种无机物,化学式Al2O3,是一种高硬度的化合物,熔点为2054℃,沸点为2980℃,在高温下可电离的离子晶体,常用于制造耐火材料。Al2O3有许多同质异晶体,已知的有10多种,主要有3种晶型,即α-Al2O3、β-Al2O3、γ-Al2O3。其中结构不同性质也不同。
存在于自然界中的氧化铝成为刚玉,是在火山爆发过程中形成的,它在岩石中呈无色的结晶体,也可与其他氧化物杂质形成带颜色的晶体,如含氧化铬的显红色称红宝石;含微量元素钛(Ti4 )或铁(Fe2 )而呈蓝色称蓝宝石。

阳极氧化膜最显著的特点是氧化膜厚度比化学氧化膜厚,其厚度约为5~30微米 ,硬质阳极氧化膜甚至可达25~150微米 ,阳极氧化膜的性质主要体现在以下几个方面:
1、透明性,阳极氧化膜未着色前是无色透明的,直接显示出底层金属的银色光泽,所以常说的本色阳极氧化实际上是省略工艺顺序中的着色阶段并直接进行阳极氧化来实现的。需要注意的是,铝的纯度越高,氧化膜的透明度就越高,所以,要取得高透明度的氧化膜,常常选用纯铝阳极氧化。
2、多孔性,在电解液中酸可局部溶解氧化膜,产生孔隙,使氧化反应得以向纵深发展,使铝的表面形成多孔结构,可使膜层对各种有机物、树脂、地蜡、无机物、染料及油漆等表现出良好的吸附能力,可进行各种着色处理,在保持金属的光泽和质感的基础上,还可以染上丰富多彩的颜色;同时也可作为涂镀层的底层,再进行其他的表面处理工艺。
3、耐磨性,阳极氧化膜较厚,且具有很高的硬度,可以提高金属表面的耐磨性。由于阳极氧化膜具有多孔性,当膜层吸附润滑剂后,能进一步提高其耐磨性。
4、耐蚀性,阳极氧化膜在大气中很稳定,因此具有较好的耐蚀性,铝在铬酸溶液中进行阳极氧化而得到的氧化膜致密、耐蚀性好;从硫酸溶液中得到的氧化膜的孔隙较前者大,不过其膜层较厚,且吸附能力很强,若经过适当的填充封闭处理,其耐蚀性也是很好的,所以膜厚和封孔质量对耐蚀性有着直接影响。
5、电绝缘性,铝本色虽然是良好的导电体,但是阳极氧化膜厚,具有很高的绝缘电阻和击穿电压,可以用作电解电容器的电介质层或电器制品的绝缘层。
6、绝热性,阳极氧化膜是一种良好的绝热层,其稳定性可达1500℃,因此在瞬间高温下工作的零件,由于氧化膜的存在,可防止铝的熔化。
7、结合力,阳极氧化膜与基体金属的结合力很强,很难用机械方法将它们分离,即使膜层随基体弯曲直至破裂,膜层与基体金属仍保持良好的结合。
三、阳极氧化的机理
阳极氧化最终的结果是氧化膜的形成,氧化膜形成的过程实际上包含两个方面:
1、成膜过程
2、溶膜过程
在这里,咋一看,感觉有点矛盾,既然需要的是成膜,为啥还需要一个溶膜过程?
别急,继续往下看,溶膜过程是很重要的。
1、成膜过程:
其原理实际上是一种电解水的原理,电解是将电流通过电解质溶液,在阴极和阳极上引起氧化还原反应的过程。
电解水的总反应为:2H2O=2H2↑ O2↑,然而这个过程并不是一步完成的,具体为: