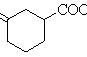
上表数据可以计算出CH3(g)+3H2(g)―→CH3(g)的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2气体时,放出的热量相等
A.①②③④⑤ B.③④⑤ C.④⑤ D.①②③⑤
解析 ①中水为气态,错误;②B具备的能量大于A,能量越高越不稳定,错误;③ΔH不随因浓度改变引起的化学平衡的移动而改变,错误;④苯环中无碳碳双键,错误;⑤金刚石和石墨不是同种物质,具备的能量不同,错误。
7、某研究小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2ONH4HCO3+NH3·H2O。测得c(NH2COO-)与反应时间的关系如图所示。据图判断下列说法正确的是( C )


解析 25 ℃时v(NH2COO-)=eq \f(2.2-1.9,6) mol·L-1·min-1=0.05 mol·L-1·min-1,C项正确。
8、关于pH相同的醋酸和盐酸溶液,下列叙述不正确的是( B )
A.取等体积的两种酸溶液分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m>n
B.取等体积的两种酸溶液分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸
C.取等体积的两种酸溶液分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸消耗的多
D.两种酸溶液中c(CH3COO-)=c(Cl-)
9、下列反应中,属于取代反应的是( B )

A.①② B.③④C.①③ D.②④
解析 反应①为加成反应,反应②为消去反应,反应③是酯化反应,反应④是苯的硝化反应,其中③④均属于取代反应。
10、下列有关实验操作的说法中,正确的是( C )
A.配制1 L 0.1 mol·L-1 NaCl溶液的实验中,用托盘天平称取5.85 g NaCl
B.用广范pH试纸测得橙汁的pH为3.50
C.用酸式滴定管量取25.00 mL高锰酸钾溶液
D.可用过滤的方法除去淀粉溶液中混有的少量NaCl杂质
解析 托盘天平的准确度为0.1 g,不能用托盘天平称取5.85 g NaCl,A项错误;pH试纸测定结果为整数,不能用广范pH试纸测得橙汁的pH为3.50,可选pH计测定,B项错误;高锰酸钾可氧化橡胶,滴定管的准确度为0.01 mL,则用酸式滴定管量取25.00 mL高锰酸钾溶液,C项正确;淀粉胶粒与离子均可透过滤纸,不能用过滤的方法除去淀粉溶液中混有的少量NaCl杂质,可选渗析法,D项错误。
11、分子组成为C6HmO3N3Cl的有机物分子中,m的最大值为( B )
A.14 B.16 C.18 D.20
解析 6个碳原子最多连有14个氢原子,O原子不增加氢原子,N原子可以看作—NH2取代了氢原子,增加1个氮原子同时增加1个氢原子,氯原子可看作取代了氢原子,最多有14+3-1=16个氢原子。
二、非选择题
(2018·江西临川质检)一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)FeO(s)+CO(g) ΔH>0,1 100 ℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2和CO的浓度与时间的关系如图所示。