初中化学里常见的四大基本反应类型是:化合反应、分解反应、置换反应、
复分解反应,现在将它们在课本及习题中的呈现形式归纳如下:
一、化合反应:由两种或两种以上的物质生成另一种物质的反应,叫化合反应。初中常见化合反应主要有:
1、非金属单质与氧气生成非金属氧化物。如 2H2 O2 = H2O
其它非金属如硫、磷、碳等都可以与氧气反应生成非金属氧化物。
2、金属与氧气反应生成金属氧化物。如 3Fe 2O2 = Fe3O4
其它金属如铝、锌、铜也可以与氧气发生类似反应,生成相应的金属氧化物。
3、金属氧化物与水反应,生成相应的碱。如CaO H2O= H2CO3,
其它金属氧化物Na2O、K2O、BaO都可以与水反应生成相应的碱
4、非金属氧化物与水反应,生成相应的酸。如 CO2 +H2O= H2 CO3
其它非金属氧化物SO2 、 SO3 也可以与水生成相应的酸。
5、其它如2CO O2 = 2CO2等。
二、分解反应:由一种物质生成两种或两种以上其他物质的化学反应叫做分解反应。初中常见分解反应有:
1、不溶性碳酸盐高温分解 如CaCO3= CaO CO2↑
2、不溶性碱受热分解,如Cu(OH)2 = CuO H2O
3、某些酸式盐受热分解如B、2NaHCO3 = Na2CO3 CO2↑ H2O
4、某些碱式盐受热分解如 Cu2(OH)2CO3 加热 2CuO CO2↑ H2O
5:其它如:2H2O2 MnO2 2H2O O2↑
2KClO3 MnO2 2KCl+ O2↑
2KMnO4 加热 K2MnO4 +MnO2+ O2↑
三、置换反应:一种单质和一种化合物生成另一种单质和另一种化合物的反应叫置换反应。初中常见反应有:
1、活泼金属与酸反应(金属为金属活动顺序中氢以前的金属,酸不包括浓硫酸和硝酸)例如Fe+2HCl=FeCl2 H2↑
Mg 2HCl = MgCl2 H2↑
H2SO4 Fe = FeSO4 H2↑
2HCl + Zn = ZnCl2 H2↑
H2SO4 Zn = ZnSO4 H2↑
2:金属与盐反应,生成新盐与新金属。盐(含较不活泼金属)+金属(较活泼)——金属(较不活泼)+盐(含较活泼金属)盐须溶于水,金属须比盐中金属活泼,钾、钙、钠三种金属不跟盐溶液发生置换反应。
如Fe+CuSO4===FeSO4 Cu 2AgNO3 + Cu= Cu(NO3)2 2 Ag
3、氢气还原金属氧化物,H2 +CuO = Cu H2O
4、碳还原金属氧化物。3C+Fe2O3 = 2 Fe 3CO2↑
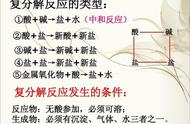
四、复分解反应:两种化合物相互交换成分,生成另外两种化合物的反应,叫复分解反应。初中常见反应有:
1、酸+碱性氧化物——盐+水
如Fe2O3+ 6HCl= 2 FeCl3 3H2O
3H2SO4 Fe2O3 = Fe2(SO4 )3 3H2O
(以上两个反应说明:HCl和H2SO4可用于除铁锈)
2HCl + CuO = CuCl2 H2O
H2SO4 CuO=CuSO4 H2O
(以上两个反应都可用于除去Cu粉中混有少量的CuO)
2HNO3 ZnO = Zn(NO3)2 H2O
H2SO4 CaO =CaSO4 H2O
2、酸+碱——盐+水(中和反应)
如HCl + KOH=KCl H2O
H2SO4 2 NaOH =Na2SO4 2 H2O
2HCl +Cu(OH)2 = CuCl2 2H2O
3 H2SO4 2Fe(OH)3=Fe2(SO4 )3 6H2O
3HCl +Al(OH)3 =AlCl3 3H2O (用Al(OH)3 治疗胃酸过多的原理)
2HNO3+Mg(OH)2=Mg Cu 2 H2O
3、 酸+盐――新酸+新盐
如HCl + AgNO3=AgCl↓ ¬ HNO3 (用于:检验Cl-;除去HNO3中的HCl)
H2SO4 + BaCl2 = BaSO4↓ 2HCl (用于:检验SO42-;除去HCl中的H2SO4)
2HCl + Na2CO3 = 2NaCl +CO2 ↑ H2O (用于:a、灭火器反应;b、检验CO32-;c、检验NaOH是否变质(Na2CO3);d、除去NaCl中的Na2CO3)
2HCl + CaCO3 = CaCl2 +CO2 ↑ H2O(用于:a、实验室制CO2;b、除去盛石灰水瓶壁上的白色固体(CaCO3)-;c、证明CaO中是否含有未完全分解的CaCO3;d、食用墨鱼骨粉(含有CaCO3)补钙的原理)
4、 碱+盐——新碱+新盐 注:反应物必须都溶于水
如2NaOH + CuSO4¬ = Cu(OH)2↓ Na2SO4 (现象:蓝色沉淀)
3NaOH + FeCl3= Fe(OH)3 ↓ 3NaCl (现象:红褐色沉淀)
Ca(OH)2 + Na2CO3= CaCO3 ↓ 2 NaOH
(工业制NaOH原理;检验NaOH是否变质(Na2CO3))
5、盐a+盐b——新盐c+新盐d 注:反应物必须都溶于水
如NaCl + AgNO3 = AgCl↓ NaNO3(用于:除去NaNO3中的NaCl)
Na2SO4 + BaCl2 = BaSO4↓ 2 NaCl(用于:除去NaNO3中的Na2SO4)
Na2CO3 + BaCl2 = BaCO3 ↓2 NaCl(用于:除去NaCl中的Na2CO3)
注意; 碱+酸性氧化物——盐+水,不属于复分解反应。
如2NaOH + CO2 = Na2CO3 H2O(NaOH在空气中变质的原因)
2NaOH + SO2 = Na2SO3 H2O(利用NaOH 溶液可吸收污染空气的SO2)
2NaOH + SO3 = Na2SO4 +H2O
Ca(OH)2 + CO2 = CaCO3 ↓ H2O(用于:a、检验CO2;b、除去CO中混有少量的CO2;c、用石灰浆抹墙会变硬的原因;d、石灰水放到空气中会产生一层白膜)
,