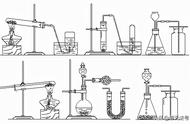
注意:集气瓶底部铺少量的细沙或加少量的水,防止生成的固体物质溅落瓶底,致使集气瓶炸裂。铁丝在空气中不能燃烧
(三)与某些化合物(蜡烛、甲烷)的反应——产物均为:二氧化碳和水
实验现象:比空气中燃烧剧烈,发出白光,集气瓶内壁出现水珠,有使澄清石灰水变浑浊的无色无味气体产生。

空气中燃烧情况:燃烧产生黄色火焰,放热,稍有黑烟。
(四)其他物质与氧气的反应
某些物质在一些条件下,与氧气发生缓慢的氧化反应,成为缓慢氧化。缓慢氧化也放热。
如:动植物新陈代谢,金属的锈蚀,食物的腐烂、酒醋的酿造、农家肥的腐熟等等。
总结:
1.氧气是一种化学性质比较活泼的气体,在一定的条件下,能与许多物质发生反应并放出大量的热。在这些反应中,氧气提供氧,称为氧化反应。氧气便是常见的氧化剂;具有氧化性。
2.物质在纯氧气中燃烧程度比空气中燃烧要剧烈。说明物质燃烧程度,与氧气的浓度大小成正比;
3.物质燃烧时有的有火焰,有的会发光,有的会冒烟。一般来说,气体燃烧会有火焰产生,固体直接燃烧,产生光或者火星。生成物有固体,一般都会产生烟,即固体小颗粒;
4.物质与氧气反应不一定是燃烧现象,如缓慢氧化。
三、氧气的用途
(1)供给呼吸:医疗上急救病人,登山、潜水、航空、宇航提供呼吸;
(2)支持燃烧:炼钢、气焊与气接、液氧炸弹、火箭助燃剂
实验室制取氧气
一、工业制法(分离液态空气法)
原理:利用液态氧和液态氮的沸点不同。——物理变化(蒸馏)
(1)具体过程

(2)注意:该过程是物理变化
二、氧气的实验室制法(化学变化)
1.双氧水(过氧化氢)制取氧气
A.药品:过氧化氢(H2O2)和二氧化锰(黑色粉末 MnO2)
B.实验原理:

注:MnO2在该反应中是催化剂,起催化作用
C.装置: 固体与液体反应,不需加热(双氧水的为一类)