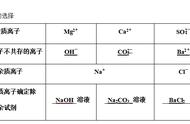
基础知识:液体的除杂
第一步:对比,找出杂质离子和非杂质离子;
第二步:找出与杂质离子不共存且不引入新杂质的离子,确定除杂试剂。
如:除去NaCl溶液中的Na2CO3如图所示:

二、粗盐中的可溶性杂质思路
1. 粗盐中的可溶性杂质为CaCl2、MgCl2以及Na2SO4,故除杂实质为除去___________________(填离子符号)。

2、方法,按照上述方法,分析出杂质离子

分析杂质离子

选择除杂试剂
流程图:

三、中考导向
1、溶解、过滤、蒸发操作中用到的实验仪器,
2、玻璃棒在不同操作中的作用。
3、除去可溶性杂质所选取的试剂
4、试剂的添加顺序及原因
5、化学方程式的书写
6、每一步反应后溶液中的溶质成分、沉淀成分。
7、每种试剂添加过量的目的。
8、加入盐酸的作用和时机
9、加入过量的盐酸不影响精盐纯度的原因。
10、最终得到的氯化钠的质量比原粗盐中氯化钠的质量大的原因。
11、加入碳酸钠的目的
12、上述流程中共有几个复分解反应
13、上述流程中过滤后的成分鉴定
14、氯化钡、氢氧化钠二者可否用一种试剂代替
,