初三化学上册知识点梳理
9年级上册化学知识点归纳(一)
1、重要的化学物质:空气、氧气、水、碳及其化合物、常见的金属、盐酸、硫酸、氢氧化钠、氢氧化钙、氯化钠、碳酸钠、碳酸氢钠、碳酸钙、化肥等。
(1)空气:空气的成分:按体积计算,氮气78%,氧气21%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%,空气是混合物。
(2)氧气:通常情况下,是无色、无味的气体,其固体和液体均为淡蓝色、 不易溶于水、 密度比空气略大(后两个性质决定了氧气的收集方法)。氧气是一种化学性质比较活泼的气体,能与许多物质发生化学反应,在反应中提供氧,具有氧化性,是常用的氧化剂。
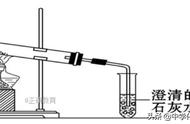
(3)二氧化碳:通常状况下为无色无味气体,固态二氧化碳(干冰)会在-78.5℃以上直接气化并吸收大量的热; 密度比空气大;能溶于水。(后两个性质决定了二氧化碳的收集方法)。一般情况下,不能燃烧,不支持燃烧也不供呼吸。 与水反应生成碳酸:CO2 H2O=H2CO3反应后的溶液使紫色石蕊试液变红。 二氧化碳与可溶性碱反应:CO2 Ca(OH)2=CaCO3↓ H2O 该反应用于检验二氧化碳。CO2 2NaOH=Na2CO3 H2O 该反应用于吸收二氧化碳。
(4)水 :由电解水生成氧气和氢气,氢气在氧气中燃烧生成水等实验都能证明水是由氢、氧两种元素组成的。构成水的粒子是水分子,一个水分子是由两个氢原子和一个氧原子构成的。
(5)金属:
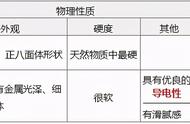
(a)共性:常温下是固体、有金属光泽、大多为热和电的良导体(用作加热器具和导线),有延展性(能展成薄片、拉成丝)、密度大、硬度大、熔点高等共性,但导电性、导热性、密度、熔点、硬度等也会存在较大的差别。
(b)特性:铁、铝等多数金属银白色,而铜为紫红色;多数为固态,而汞为液态等。 (c)合金:在金属中加热熔合某些金属或非金属,就可以制得具有金属特征的合金。合金的强度、硬度和抗腐蚀性一般比组成它们的纯金属要好,有更广泛的用途,生活中大量使用的不是纯金属而是合金,如生铁和钢;钛和钛合金等等。钢和生铁都是铁碳合金,生铁的含碳量为2%—4.3%,钢的含碳量为0.03%—2%。
(d)金属的化学性质因它们的活泼性不同而有较大差异,要掌握常见金属与氧气、与酸的反应。
(e)有关酸碱盐部分重点是掌握盐酸、稀硫酸的化学性质和酸的通性,掌握氢氧化钠、氢氧化钙的化学性质和碱的通性,掌握常见盐的化学性质及用途,理解复分解反应发生的条件。
2、物质构成的奥秘:分子、原子、离子、元素
宏观物质都是由微观粒子构成的。分子、原子、离子都是构成物质的粒子。
(1) 分子的定义:
分子是保持物质化学性质的最小粒子。
提示:分子在物理变化中不可分,分子间的距离可变化;分子在化学变化中可分,分子中的原子可重新组合,构成新的分子。
9年级上册化学知识点归纳(二)
一、认识质量守恒定律,认识常见反应中的质量关系
(1)铁钉生锈后质量为什么增加?
(2)高锰酸钾加热一段时间后,剩余固体质量为什么减少?
二、用微观的观点对质量守恒定律作出解释
(1)知道质量守恒的微观原因?
(2)会推断未知物质的化学式(注意有无系数)
三、探究化学反应中的质量关系
在什么情况下,必须在密闭体系中进行实验。
四、能正确书写简单的化学方程式
(1)查化学式 --- 根据化合价;
(2)查配平 --- 数原子数,尤其氧原子;
(3)查条件和箭头 ---- 根据所学知识或题目所给信息。
五、能根据化学方程式进行简单的计算
(1)化学方程式的配平必须要查;
(2)比例式必须要列;
(3)设答必须要完整;
(4)单位,x---不带单位,数字---必须带。
9年级上册化学知识点归纳(三)
一、原子的构成
(1)知道原子是由原子核和核外电子的构成?
(2)原子是由哪几种粒子构成的?它们是怎样构成原子的?为什么整个原子不显电性?原子的空间分布和质量分布分别有什么特点?
二、记住一些常见元素的名称和符号 自然界的水 物质构成的奥秘
三、知道元素的简单分类
元素可以分为哪三类?分类的依据是什么?不同类别的元素的最外层电子数和化学性质各有什么特点?
四、能根据原子序数在元素周期表中找到指定的元素,如:8、18、28、38、48等
五、形成“化学过程中元素不变”的观念
化学反应前后,元素的种类和质量是否改变?微观原因是什么?
六、核外电子
初步认识核外电子在化学反应中的作用,为什么说最外层电子数决定元素的化学性质?
七、原子与离子
知道同一元素的原子和离子可以相互转化。如:Na与Na 、S与S2-如何相互转化?在转化过程中,质子数、中子数、最外层电子数变化情况?知道离子是构成物质的微粒,NaCl是由什么粒子构成的?
八、说出几种常见元素和原子团的化合价
K、Na、Ca、Zn、Mg、Cl、Al、SO4、OH、NO3、NH4、CO3等。
九、能用化学式表示常见物质的组成
(1)根据俗名写化学式;(2)根据用途写化学式;(3)根据化合价写化学式。
十、能利用相对原子质量、相对分子质量进行物质组成的简单计算
(1)计算相对分子质量;(2)计算元素间的质量比;(3)计算某一元素的质量分数;
(4)根据计算来确定有机物的组成中除C、H元素之外是否含有氧元素;
当 M有机物 等于 MH MC 不含有O元素;
大于 MH MC 含有O元素;差值即为氧元素的质量。
十一、能懂商品标签上的物质成分及含量
(1)要注意标示的是物质的质量还是元素的质量,如:加钙盐CaCO3-Ca,加碘盐KIO3-I;
(2)要注意标示的单位质量与所给的质量或体积单位是否一致。
十二、能根据某种氮肥包装袋或产品说明书标示的含氮量推算它的纯度
(1)标示的含氮量 实际含氮量(不纯)
根据化学式计算含氮量 理论含氮量(纯)则纯度=实际含氮量/理论含氮量×100%
(2)判断广告其真实性
若标示的含氮量 大于 理论含氮量 则是虚假广告。
十三、平均值问题
两种不等量物质混合,所得实际结果必介于两种之间。
,