金刚石是硬度很高的原子晶体,导电性和导热性都很差。金刚石中每个碳以sp3杂化形式形成4个sp3杂化轨道,相邻碳原子之间以sp3杂化轨道相互重叠形成共价键,所有的碳原子之间均已共价键连接形成一个大分子,晶体为原子晶体,导电性和导热性都很差;
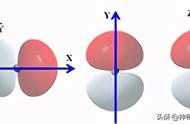
石墨是典型的层状结构晶体,具有良好的导电性,传热性和延展性。石墨在层面上每个碳原子以sp2杂化形式形成3个sp2杂化轨道,分别与相邻的3个碳原子形成3个sp2-sp2重叠的键,键角为120度,从而得到由许多正六边形构成的平面结构。在平面中的每个碳原子还有1个2p原子轨道垂直于sp2杂化轨道,每个2p轨道中还有1个电子,有这些相互平行的2p轨道相互重叠可以形成遍及整个平面层的离域大p键。由于大p键的离域性,电子能沿平面层方向移动,使石墨有很好的导电性和传热性。在石墨晶体中,相邻层间距较大,作用力为分子间力,故石墨层间易滑动。
2.往离心试管中加入少量0.1mol∙dm-3AgNO3溶液,然后按以下次序进行试验。写出每一步骤实验现象和相关的反应方程式。(12分)(每空一分)
实验步骤 | 实验现象 | 反应式 |
滴加0.1mol∙dm-3NaCl溶液至刚生成沉淀 | 有白色沉淀生成 | Ag Cl- = AgCl |
滴加6mol∙dm-3氨水溶液至沉淀刚溶解完 | 白色沉淀溶解 | AgCl 2NH3·H2O = [Ag(NH3)2] 2H2O Cl- |
滴加0.1mol∙dm-3KBr溶液至沉淀刚生成沉淀 | 有浅黄色沉淀生成 | [Ag(NH3)2] Br- = AgBr 2NH3 |
滴加1mol∙dm-3Na2S2O3溶液至沉淀刚溶解完 | 浅黄色沉淀溶解 | AgBr 2S2O32-(稀) = [Ag(S2O3)2]3- Br- |
滴加0.1mol∙dm-3KI溶液至刚生成沉淀 | 有黄色沉淀生成 | [Ag(S2O3)2]3- I - = AgI 2S2O32- |
滴加饱和Na2S2O3溶液至沉淀刚溶解完 | 黄色沉淀溶解 | AgI 2S2O32-(浓)= [Ag(S2O3)2]3- I - |
四、计算题(本大题共3小题,共28分)
1.已知在298.15K下,8.0mol SO2和4.0 mol O2在密闭容器中进行反应生成SO3气体,测得起始时和平衡时(温度不变)系统的总压力分别为300kPa和220kPa,计算该温度时反应:2SO2 O2 = 2SO3的SO2的转化率、标准平衡常数和该温度下的

(共10分)
解:设平衡时SO3的物质的量为x mol
2SO2 (g) O2(g) = 2SO3(g)
起始时物质的量/mol 8.0 4.0 0
平衡时物质的量/mol 8.0-x 4.0-x/2 x (1分)
在恒温恒容条件下,系统总压与系统的总物质的量成正比,故
300kPa :220kPa = (8.0 4.0) :(8.0-x 4.0 – x/2 x) (1分)
x = 6.4 (1分)
SO2 的转化率a =

(1分)
平衡时总的物质量 n总 = 8.0-x 4.0 – x/2 x = 8.8 (mol) (0.5分)
各物质的平衡分压为
peq(SO2) =[ (8.0-6.4)/8.8]×220kPa = 40kPa (0.5分)
peq(O2) =[ (4.0-6.4/2)/8.8]×220kPa = 20kPa (0.5分)
peq(SO3) =(6.4/8.8)×220kPa = 160kPa (0.5分)
Kq =