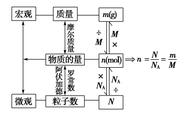
物体含有物质的多少叫质量,它不随物体形状、状态和空间位置的改变而改变,是物质的基本属性。它与重力无关,比如,一个物体在地球上与在月球上的重量不同,但质量还是不变的。
这段话很正确,但除了靠记忆背诵或者自己去悟之外,并不能让学生理解什么是质量,假使我们从微观角度去解析,将能深刻把握质量这一重要的物理概念。
我们知道,物质由分子组成,组成分子的单位是原子,即不同元素的原子以共价键的形式形成分子,而分子则构成了丰富多彩的万物世界。
先说化学课讲到的元素,以我们常见的物质水、空气(氮气和氧气等)和铁为例,最小的元素是氢H原子,相对质量我们规定为1,相对较重有氮原子N(相对质量是14)、氧原子(相对质量是16),这几个中元素最重的是铁原子Fe(相对质量是56);而实际的水分子H2O相对质量是18;氧气分子O2相对质量是32,氮气分子N2相对质量是28,铁分子也是一个铁原子Fe相对质量仍是56。
以上数据咋一看,怎么氧气、氮气分子还比水分子重?为什么其真实的密度(同体积下质量)要比水轻很多呢?
要搞清这个问题,须回答如下问题,
(1)真实客观的微观粒子中,原子、分子尤其分子的质量和体积是多少呢?
这还得从化学单位说起。
1摩尔(mol)任何理想气体在标况下(一个大气压、0摄氏度)的体积是22.4升,而我们科学测定1mol的气体有约6.02x10^23(这个大数叫作阿伏伽德罗常数)个分子,也就是说,1mol氧气约有6千万亿亿个氧气分子O2;同样1mol水约有6千万亿亿个水分子H2O。
为了比较形象地比较大小,我们脑海里可产生一个理想实验(实际上不容易做到):在标况下我们用一个密闭的袋子装满水,然后让这个袋子体积扩张,一部分水变成了水蒸气填补了增加的空间,正好得到1mol的水和1mol的水蒸气。经测量,1mol水的质量是18g,体积是18毫升,空间里的水蒸气体积是22.4升。
数学计算:
1个水分子H2O的质量和体积是,
18/6.02*10^23=3*10^-23 (g)
或18/6.02*10^23=3*10^-23 (ml)
即3千万亿亿分之一克或毫升。
1个水蒸气分子H2O的质量和体积是,
质量应与水分子相同,仍为3*10^-23 (g);
体积:22.4/6.02*10^23=3.8*10^-23 (l)
(2)固液体与气体密度差别如此大的原因是什么?
由于分子有大有小,尤其有机物大分子不好算,物理教材里没有把这些细节讲清楚。真实情况是,大约水分子的直径与水分子之间的间隙在一个数量级,以分子之间的间隙等于分子尺寸粗略计,如把间隙也想象成另一种与水分子尺寸相当的分子,那么水分子真实体积是其占用空间的1/2,那么空隙占用空间也为1/2(只是估计粗略数据,不是真实准确数据);因为分子之间相互耦合,其间隙也是不可压缩的,比如,1万米以下的海沟处的水被压缩的压力达到1000个大气压,但水的密度增加几乎可以忽略。根据以上一个水蒸气占用体积与一个水分子占用体积来计算:
3.8*10^-23 (l)/3*10^-23 (ml)
=1300倍(相当于一个1300立方当量体积内只有一个水蒸气分子)
这样估算,水蒸气分子之间的间距是其水分子直径的11-1=10倍。
也就是说,水分子之间有间隙,但几乎不可压缩,这是由分子结构决定的,除非其原子被压缩成了中子,空间进一步被压缩一定极限还有可能变成黑洞的组成物质。
水蒸气体积在高压下可以从原有蒸气体积压缩到1000分之一左右,分子之间的距离变为原水蒸气分子间距的1/10,间隙回到与分子直径一个数量级,即与液态时水分子之间的间隙相当。
粗略计算后总结为,物质密度之所以不同,跟组成物质的分子的质量与分子占有体积相关,固态物质还跟晶体结构排列形成的间隙相关,即跟物质致密程度相关;
而气体体积之所以这么大,是因为其分子的间距是分子尺寸的10倍左右,空隙占了绝大部分体积,导致分子的体积与其分子本身的结构关系不大,只与压力和温度相关,即1mol理想气体如氮气、氧气、空气或者水蒸气等在标况下的体积都是22.4升。
附图:用数学计算去认识物理世界