大肠杆菌引起的食物中毒可导致出血性腹泻和肾脏损伤,可谓最严重的食物中毒类型之一。但美国研究者指出,这些可怕的后果可能只是感染后的外在表现。他们发现了特定大肠杆菌入侵免疫系统的新机制,而其中的关键是志贺毒素,相关研究发表于《科学—免疫学》。
大肠杆菌生活在多种动物的肠道中,其中少部分会在特定条件下引发疾病,比如胃肠道感染。一些大肠杆菌还可能引起尿路感染甚至败血症。
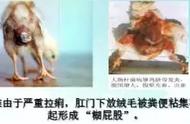
其中能产生志贺毒素的大肠杆菌毒性严重,其引发的感染会导致腹泻、发热,严重感染者可能死亡。幼儿感染后会引起急性中毒,大约15%的幼儿患者因此患肾脏疾病,还有一部分幼儿的肾脏可能会受到长期损伤。
在产生志贺毒素的大肠杆菌中,有一类亚型被称为肠出血性大肠杆菌(EHEC)。这种亚型常见于反刍动物的肠道中,比如牛。未经合格卫生处理的牛肉含有的EHEC很可能导致人体感染。
近年来,通过严格限制屠宰场的处理流程,此类情况有所改善,但危险仍然存在,比如含有牛粪便的液体流经的屠宰场附近的田地,以牛粪为肥料浇灌的蔬菜都有可能出现EHEC。
对人类而言,感染EHEC后往往难以治疗,如果抗生素使用不当,反而会让这些濒死的细菌产生更多志贺毒素。感染EHEC早期,人体免疫系统的相应部分会做出反应,但EHEC非常擅长攻击这部分免疫系统,抑制其发出信号,从而在人的肠道中不受控制地生长。因此,关键在于如何阻止这种细菌进入体内。
康涅狄格大学健康中心免疫学家Shivapriya Vanja与其课题组博士后研究员Morena Havira等人在论文中揭示了EHEC对抗免疫系统的机制。
在人体免疫系统中,通过感知胞质脂多糖(LPS)并与之结合,炎性细胞凋亡蛋白酶可以启动相应的分子功能并触发细胞凋亡,让外来细菌受损,这一流程是免疫系统防御后者入侵的重要机制。
但当EHEC入侵时,这一防御机制被破坏了。为了弄清EHEC如何破坏免疫防线,研究小组从细菌库中提取了许多不同种类的EHEC,并让其感染免疫细胞。
研究小组发现,EHEC在感染宿主期间,其表达的志贺毒素会抑制消皮素D的活性,进而抑制由受体蛋白酶Caspase-11(一种非经典炎症小体)介导的胞质LPS感知机制。此外,多种志贺毒素变体都会抑制小鼠及人体细胞中的胞质LPS感知机制。
除了发现新的作用机制外,这是科学家首次发现志贺毒素可以破坏炎性小体。为了进一步找到志贺毒素产生抑制作用的具体原因、寻找抵抗这种抑制作用的药物,研究小组正在开展后续研究。(袁柳)
来源: 《中国科学报》
,