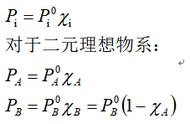vB气体物质计量系数的代数和(公式5) ΔrHm、ΔrUm与化学计量数有关。 (3)热力学标标准状态:在温度T 和标准压力pθ(100kPa)下的物质的状态。(通常采用T=298.15K) • 液体和固体的标准态:指定温度、标准压力下的纯固体和纯液体。(若有不同形态则选最稳定的形态) • 气体的标准态:指定温度、标准压力下具有理想气体性质的状态(气体混合物中,各气体分压均为标准压力)。 • 溶液中溶质的标准态:指定温度、标准压力下的物质的质量摩尔浓度mb= 1mol。kg-1理想稀溶液性质的状态。 标准热力学函数:标准状态时热力学函数。ΔrHmθ为标准摩尔反应焓变 (4)热化学方程式 注明是等压热效应还是等容热效应,前者用ΔrHm表示后者用ΔrUm,表示。(吸热反应为正,放热反应为负。) • 注明反应的温度和压力。 • 注明物质的聚集状态和晶型。g、l、s分别表示气、液、固态;用aq表示水溶液。 注明反应的计量方程式,计量方程式不同,摩尔反应焓也不同。 6、化学反应热效应的计算 (1)盖斯定律 在恒温恒压条件下,系统只做体积功时,化学反应的热效应只与反应的始态和终态有关,而与反应的途径无关。 (2)标准摩尔生成焓 1)定义:在标准状态下,由最稳定单质生成1mol化合物时的热效应称为该物质的标准摩尔生成焓。ΔfHmθ单位kJ·mol-1 ;温度一般取298.15K,ΔfHmθ(稳定单质)= 0(C的稳定单质为石墨,磷的稳定单质为白磷) 2)

(公式6) (3)标准摩尔燃烧焓 1)定义:在标准状态下,1mol物质完全燃烧时的反应焓变称为该物质的标准摩尔燃烧焓。 符号:ΔcHmθ;单位kJ·mol-1;温度一般298.15K • 完全燃烧:物质中的碳、氢、硫完全转变成CO2(g),H2O(l)和SO2(g)。 • O2完全燃烧产物的ΔcHmθ = 0。 2)

(公式7) 3)ΔrHm(TK)≈ΔrHm(298.15K) 三、热力学第二定律 1、热力学第二定律 1)、自发过程的不可逆性 ①自发过程有明显的方向性。②自发过程有一定的限度。③自发过程有对外做功的能力。④自发过程的不可逆性。 2)热力学第二定律两种表述: 开尔文说法——不可能从单一热源取热,使之完全变为功而不引起其它的变化。(功变热的不可逆性) 克劳修斯说法——不可能使热从低温物体传递到高温物体而不引起其它变化。(热传导的不可逆性) 不是说热不能变成功,但需从两个热源取热全部变成功。 不是说不能从单一热源取热全部变成功,而是强调会产生其它影响。 3)热力学第二定律数学表达式 熵的定义:dS=

熵S是状态函数。单位J·K-1 摩尔熵Sm 单位J·K-1 ·mol-1 熵的物理意义:系统无序程度或混乱度的量度。 热力学第二定律数学表达式: