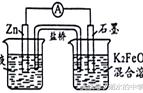
过氧化氢分解
②氧化性:在酸性介质中,可氧化一些金属或低价金属离子
如:2Fe2++H2O2+2H+===2Fe3++2H2O、Cu H2O2 2H =Cu2+ 2H2O
③弱还原性:遇到强氧化剂时表现还原性,
如:2Mn04— 5H2O2 6H+=2Mn2 5O2↑ 8H2O、H2O2 Cl2=2HCl O2
④弱酸性:H2O2是二元弱酸,H2O2⇌H+ HO2-、HO2-⇌H+ O22-
可与碱反应:H2O2 Ba(OH)2=BaO2 2H2O
3、化工生产的作用:绿色氧化剂,分解产物还原产物无污染、无毒、不腐蚀设备。
良好的消毒*菌剂或漂白剂

双氧水可医用、浓度一般是2.5%

医用过氧化氢可以处理伤口
4、过氧化氢蒸气或雾对呼吸道有强烈的腐蚀性。会对眼造成不可逆损伤或失明。爆炸性强氧化剂,与可燃物反应放出大量热和氧气而引起着火爆炸。
【练习巩固】