强调之一是用等号,强调之二是标明胶体而不是沉淀,强调之三是加热。
3、命题角度:配制步骤及对应离子方程式的书写
三、焰色反应:1、 步骤:洗—烧—蘸—烧—洗—烧
2 、该实验用铂丝或铁丝
3 、焰色反应可以是单质,也可以是化合物,是物理性质
4 、Na ,K 的焰色:黄色,紫色(透过蓝色的钴玻璃)
5 、某物质作焰色反应,有黄色火焰一定有Na ,可能有K
6、命题角度:实验操作步骤及Na ,K 的焰色
四、Fe(OH)2的制备:1、实验现象:
白色沉淀立即转化灰绿色,最后变成红褐色沉淀。
2、化学方程式为:
Fe2 2OH-=Fe(OH)2
4e(OH)2 O2 2H2O= 4e(OH)3
3、注意事项:
(1)所用亚铁盐溶液必须是新制的,NaOH溶液必须煮沸,
(2)滴定管须插入液以下,
(3)往往在液面加一层油膜,如苯或食物油等(以防止氧气的氧化)。
4、命题角度:
制备过程中的现象、方程式书写及有关采取措施的原因
五、硅酸的制备:1、步骤:
在试管中加入3—5mL饱和Na2SiO3溶液,滴入1—2滴酚酞溶液,再用胶头滴管逐滴加入稀盐酸,边加边振荡,至溶液颜色变浅并接近消失时停止。
2、现象:
有透明的硅酸凝胶形成
3、化学方程式:
NaSiO3 2HCl= H2SiO3↓ 2NaCl(强酸制弱酸)
4、 NaSiO3溶液由于SiO32-水解而显碱性,从而使酚酞试液呈红色。
六、重要离子的检验:1、Cl-的检验:
加入AgNO3溶液,再加入稀硝酸,若生成不溶于稀HNO3的白色沉淀;或先加硝酸化溶液(排除CO32-干扰),再滴加AgNO3溶液,如有白色沉淀生成,则说明有Cl-存在
2、SO42-的检验:
先加入盐酸,若有白色沉淀,先进行过滤,在滤液中再加入BaCl2溶液,生成白色沉淀即可证明。若无沉淀,则在溶液中直接滴入BaCl2溶液进行检验。
命题角度:检验方法、除杂、沉淀洗涤及相关纯度的计算
七、氨气的实验室制法1、反应原理 :
2NH4Cl Ca(OH)2 ==CaCl2 2NH3↑ 2H2O
2、收集:
向下排空气法(管口塞一团棉花,避免空气对流)
3、验满:
①将湿润的红色石蕊试纸放在试管口,若试纸变蓝,说明氨气已收集满
②将蘸有浓盐酸的玻璃棒靠近试管口,出现大量白烟,则证明氨气已收集满
4、干燥方法:
碱石灰干燥(不能无水氯化钙)
5、装置图:
固体和固体加热制气体的装置,与制氧气的相同
拓展:浓氨水或浓铵溶液滴到生石灰或烧碱中制氨气,或浓氨水直接加热也可制氨气

6、命题角度:
因氨气作为中学化学实验制取气体中唯一的实验,其地位不可估量。主要角度为:反应原理、收集、干燥及验满等,并以此基础进行性质探究实验。
八、喷泉实验1、实验原理:
氨气极易溶于水,挤压胶头滴管,少量的水即可溶解大量的氨气(1:700),使烧瓶内压强迅速减小,外界大气压将烧杯中的水压入上面的烧瓶,故NH3、HCl、HBr 、HI、 SO2 等气体均能溶于水形成喷泉。
2、实验现象:
产生红色喷泉(氨气溶于水形成碱性溶液,酚酞遇碱显红色)
3、实验关键:
①氨气应充满 ②烧瓶应干燥 ③装置不得漏气
4、实验拓展:
CO2、H2S、Cl2等与水不能形成喷泉,但与NaOH溶液可形成喷泉


1、实验原理:
Cu 2H2SO4(浓)==CuSO4 SO2↑ 2H2O
2、现象:
加热之后,试管中的品红溶液褪色,
或试管中的紫色石蕊试液变红;
将反应后的溶液倒入盛有水的烧杯中,溶液由黑色变成蓝色。
3、原因解释:
变黑的物质为被浓硫酸氧化生成CuO,CuO与冲稀的硫酸反应生成了CuSO4溶液。
【提示】
由于此反应快,利用铜丝,便于及时抽出,减少污染。
命题角度:SO2的性质及产物的探究、“绿色化学”及尾气的处理等。
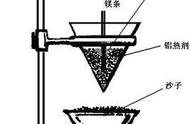
十、铝热反应: