一、燃烧的概念
可燃物与空气中氧气发生的一种发光、放热的剧烈的氧化反应。
二、燃烧的条件
(1)可燃物
(2)氧气(或空气)
(3)温度达到着火点
注意:三者缺一不可,否则不能燃烧。
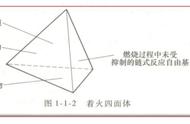
1、实验:如右图所示:

A、薄铜片上的白磷燃烧而红磷不燃烧,说明了燃烧需要温度达到着火点;
B、薄铜片的白磷燃烧而水中的白磷不燃烧,说明了燃烧需要氧气;
C、白磷的着火点低,应贮存在装有水的试剂瓶中
2、 燃烧与缓慢氧化的比较:
相同点:都是氧化反应、都放热;
不同点:前者发光、反应剧烈;后者不发光、反应缓慢。
三、灭火的原理及方法
1、燃烧的条件决定着灭火的原理,只要破坏燃烧的任何一个条件,就可以达到灭火的目的
2、灭火的原理:(1)消除可燃物(2)隔绝氧气(或空气)(3)降温到着火点以下。
3、泡沫灭火器:
扑灭木材、棉布等燃烧引起的失火。
干粉灭火器:扑灭一般的失火外,还可以扑灭电器、油、气等燃烧引起的失火。
液态二氧化碳灭火器:扑灭图书、档案、贵重设备、精密仪器等处的失火
4、泡沫灭火器的反应原理:利用碳酸钠与浓盐酸迅速反应产生大量的二氧化碳来灭火
化学反应方程式:Na2CO3 2HCl=2NaCl H2O CO2↑
常见灭火的方法 ① 油锅着火,用锅盖盖灭
② 电器着火,先应切断电源
③ 煤气泄漏,先应关闭阀门,再轻轻打开门窗,切忌产生火花
④ 酒精在桌面上燃烧,用湿抹布扑盖
⑤ 扑灭森林火灾,将大火蔓延前的一片树木砍掉
其它:
A、生煤炉火时,需先引燃纸和木材,因为纸和木材的着火点比煤低,容易点燃;
B、室内起火,如果打开门窗,会增加空气的流通,增加氧气的浓度,反应剧烈,燃烧更旺;
C、用扇子扇煤炉火,虽然降低了温度,但没有降至着火点以下,反而增加了空气的流通,所以越扇越旺;
D、用扇子扇蜡烛火焰,虽然增加了空气的流通,但却降低了温度至着火点以下,所以一扇就灭。
四、爆炸与燃烧的区分
概 念 | 发生条件 | 防范措施 | |
燃 烧 | 可燃物与氧气发生的一种发光、发热的剧烈的氧化反应 | 可燃物;与空气或氧气接触;温 度达到着火点 | 可燃物与其他物品隔离;与空气隔离;降低温度至着火点以下 |
爆 炸 | 可燃物在有限的空间内发生急剧燃烧,短时间内积聚大量的热,使气体体积迅速膨胀而引起爆炸 | 剧烈燃烧;有限空间 | 严禁烟火 |
缓慢氧化 | 反应进行得很慢,甚至不易 察觉的氧化反应 | 与空气或氧接触 |
注意:
① 爆炸可能是化学变化(如:火药爆炸)也可能是物理变化(如:车胎爆炸)。
② 化学变化的爆炸:可燃物在有限空间内急速燃烧,放出的热使气体的体积迅速膨胀。
③ 可燃性气体(氢气、一氧化碳、甲烷)或粉尘(面粉、煤粉)与空气或氧气混合,遇到明火可能会发生爆炸;可燃性气体在点燃或加热前都要验纯,以防止发生爆炸。
④ 油库、面粉加工厂门口贴有“严禁烟火”的标志:空气中常混有可燃性气体或粉尘,接触到明火,就有发生爆炸的危险。
⑤ 可燃物与氧气的接触面积越大,燃烧越剧烈。
,