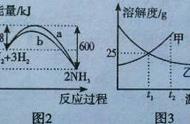
3.【2017新课标3卷】短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。下列关系正确的是
W | X | |||
Y | Z |
A.氢化物沸点:W<Z B.氧化物对应水化物的酸性:Y>W
C.化合物熔点:Y2X3<YZ3 D.简单离子的半径:Y<X

【答案】D
【解析】设W原子的最外层电子数为x,由图表可知,四种元素原子的最外层电子数之和=x x 1 x-2 x 2=21,解得x=5,则W为N元素、X为O元素、Y为Al元素、Z为Cl元素。A.NH3分子间有氢键,其沸点比HCl高,故A错误;B.Al(OH)3显两性,N元素的氧化物对应的水化物HNO3、HNO2均显酸性,故B错误;C.Al2O3是离子晶体,高熔点,而AlCl3是分子晶体,熔点低,故C错误;D.Al3 和O2-离子结构相同,核电荷数大,离子半径小,故D正确。答案选D。
【名师点睛】考查元素周期表的结构及元素周期律的应用,其中微粒的半径大小比较是该题的难点,比较方法是:(1)同周期元素的微粒:同周期元素的原子或最高价阳离子或最低价阴离子半径随核电荷数增大而逐渐减小(稀有气体元素除外),如Na>Mg>Al>Si,Na >Mg2 >Al3 ,S2->Cl-;(2)同主族元素的微粒:同主族元素的原子或离子半径随核电荷数增大而逐渐增大,如Li<Na<K,Li <Na <K ;(3)电子层结构相同的微粒:电子层结构相同(核外电子排布相同)的离子半径(包括阴、阳离子)随核电荷数的增加而减小,如O2->F->Na >Mg2 >Al3 ;(4)同种元素形成的微粒:同种元素原子形成的微粒电子数越多,半径越大,如Fe3 <Fe2 <Fe,H <H<H-;(5)电子数和核电荷数都不同的,可通过一种参照物进行比较,如比较Al3 与S2-的半径大小,可找出与Al3 电子数相同的O2-进行比较,Al3 <O2-,且O2-<S2-,故Al3 <S2-。