化学式
无机部分:
纯碱、苏打、天然碱、口碱:Na2CO3
小苏打:NaHCO3
大苏打:Na2S203
石膏(生石膏):CaSO4.2H2O
熟石膏:2CaSO4..H2O
莹石:CaF2
重晶石:BaSO4(无毒)
碳铵:NH4HCO3
石灰石、大理石:CaCO3
生石灰:CaO
熟石灰、消石灰:Ca(OH)2
食盐:NaCl
芒硝:Na2SO4.7H2O(缓泻剂)
烧碱、火碱、苛性钠:NaOH
绿矾:FaSO4.7H2O
干冰:CO2
明矾:KAI (SO4)2·12H2O
漂白粉:Ca (ClO)2、CaCl2(混和物)
泻盐:MgSO4·7H2O
胆矾、蓝矾:CusO4.5H2O
双氧水:H2O2
皓矾:ZnSO4.7H2O
硅石、石英:SiO2
刚玉:Al203
水玻璃、泡花碱、矿物胶:Na2SiO3
铁红、铁矿:Fe203
磁铁矿:Fe304
黄铁矿、硫铁矿:FeS2
铜绿、孔雀石:Cu2(OH)2CO3
菱铁矿:FeCO3
赤铜矿:Cu2O
波尔多液:Ca(OH)2和CuSO4
石硫合剂:Ca (OH)2和S
玻璃的主要成分:Na2SiO3、CaSiO3、SiO2
过磷酸钙(主要成分):Ca (H2PO4)2和CasO4
重过磷酸钙(主要成分):Ca (H2PO4)2
天然气、沼气、坑气(主要成分):CH4
水煤气:CO和H2
硫酸亚铁铵(淡蓝绿色):Fe (NH4)2(SO4)2 溶于水后
呈淡绿色
光化学烟雾:NO2在光照下产生的一种有毒气体
王水:浓HNO3与浓HCI按体积比1:3混合而成。
铝热剂:AI Fe2O3或其它氧化物。
尿素:CO(NH2) 2
有机部分:
氯仿:CHCI3
电石:CaC2
电石气:C2H2(乙炔)
TNT:三硝基甲苯
酒精、乙醇:C2H50H
氟氯烃:是良好的制冷剂,有毒,但破坏03层。
醋酸:冰醋酸、食醋 CH3COOH
裂解气成分(石油裂化):烯烃、烷烃、炔烃、H2S、
CO2、CO等。
甘油、丙三醇:C3H803
焦炉气成分(煤干馏):H2、CH4、乙烯、CO等。
石炭酸:苯酚
蚁醛:甲醛HCHO
福尔马林:35%—40%的甲醛水溶液
蚁酸:甲酸 HCOOH
葡萄糖:C6H1206
果糖:C6H1206
蔗糖:C12H22011
麦芽糖:C12H22011
淀粉:(C6H1005)n
硬脂酸:C17H35COOH
油酸:C17H33COOH
软脂酸:C15H31COOH
草酸:乙二酸 HOOC—COOH 使蓝墨水褪色,强酸
性,受热分解成CO2和水,使KMnO4酸性溶液褪
色。
化学现象
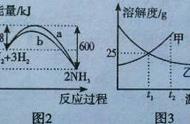
1、铝片与盐酸反应是放热的,Ba(OH)2与NH4CI反
应是吸热的
2、Na与H2O(放有酚酞)反应,熔化、浮于水面、转
动、有气体放出(熔、浮、游、嘶、红)
3、焰色反应:Na黄色、K紫色(透过蓝色的钴玻
璃)、Cu 绿色、Ca砖红、Na (黄色)、K (紫色)
4、Cu丝在Cl2中燃烧产生棕色的烟
5、H2在Cl2中燃烧是苍白色的火焰
6、Na在CI2中燃烧产生大量的白烟
7、P在Cl2中燃烧产生大量的白色烟雾
8、SO2通入品红溶液先褪色,加热后恢复原色
9、NH3与HCI相遇产生大量的白烟
10、铝箔在氧气中激烈燃烧产生刺眼的白光
11、镁条在空气中燃烧产生刺眼白光,在CO2中燃烧
生成白色粉末(MgO),产生黑烟
12、铁丝在Cl2中燃烧,产生棕色的烟
13、HF腐蚀玻璃:4HF SiO2 =SiF4 2H2O
14、Fe(OH)2在空气中被氧化:由白色变为灰绿最后
变为红褐色
15、在常温下:Fe、AI 在浓H2SO4和浓HNO3中钝
化
16、向盛有苯酚溶液的试管中滴入FeCl3溶液,溶液
呈紫色;苯酚遇空气呈粉红色
17、蛋白质遇浓HNO3变黄,被灼烧时有烧焦羽毛气
18、在空气中燃烧:
S——微弱的淡蓝色火焰
H2——淡蓝色火焰
H2S——淡蓝色火焰
CO——蓝色火焰
CH4——明亮并呈蓝色的火焰
S在O2中燃烧——明亮的蓝紫色火焰。
19.特征反应现象:
20.浅黄色固体:S或Na2O2或AgBr
21.使品红溶液褪色的气体:SO2(加热后又恢复红
色)、CI2(加热后不恢复红色)
22.有色溶液:
Fe2 (浅绿色)
Fe3 (黄色)
Cu2 (蓝色)
MnO4-(紫色)
有色固体:
红色(Cu、Cu20、Fe2O3)
红褐色[Fe(OH)3]
黑色(CuO、FeO、FeS、CuS、Ag2S、PbS)
蓝色[Cu(OH)2]
黄色(Agl、Ag3PO4)
白色[Fe(0H)2、CaCO3、BaSO4、AgCI、BasO3]
有色气体:
Cl2(黄绿色)
NO2(红棕色)
元素的一些特殊性质
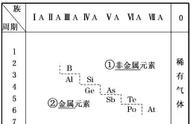
1.周期表中特殊位置的元素
①族序数等于周期数的元素:H、Be、Al、Ge.
②族序数等于周期数2倍的元素:C、S。
③族序数等于周期数3倍的元素:O。
④周期数是族序数3倍的元素:Li,Ca。
⑤周期数是族序数3倍的元素:Na、Ba。
⑥最高正价与最低负价代数和为零的短周期元素:C
⑦最高正价是最低负价绝对值3倍的短周期元素:S.
⑧除H外,原子半径最小的元素:F。
⑨短周期中离子半径最大的元素:P。
2.常见元素及其化合物的特性
①形成化合物种类最多的元素、单质是自然界中硬度最大的物质的元素或气态氢化物中氢的质量分数最大的元素:C。
②空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N。
③地壳中含量最多的元素、气态氢化物沸点最高的元素或氢化物在通常情况下呈液态的元素:O。
④最轻的单质的元素:H;最轻的金属单质的元素:Gi。
⑤单质在常温下呈液态的非金属元素:Br;金属元素:Hg 。
⑥最高价氧化物及其对应水化物既能与强酸反应,又能与强碱反应的元素:Be、Al、Zn。
⑦元素的气态氢化物和它的最高价氧化物对应水化物能起化合反应的元素:N;能起氧化还原反应的元素:S。
⑧元素的气态氢化物能和它的氧化物在常温下反应生成该元素单质的元素:S。
⑨元素的单质在常温下能与水反应放出气体的短周期元素:Li、Na、F.
⑩常见的能形成同素异形体的元素:C、P、O、S。
化学考试常用规律
1、溶解性规律——见溶解性表;
2、常用酸、碱指示剂的变色范围:

3、在惰性电极上,各种离子的放电顺序:
阴极(夺电子的能力):
Au3 >Ag >Hg2 >Cu2 >Pb2 >Fa2 >Zn2 >H >Al3 >Mg2 >Na >Ca2 >K
阳极(失电子的能力):S2->I->Br->Cl->OH->含氧酸根
注意:若用金属作阳极,电解时阳极本身发生氧化还原反应(Pt、Au除外)
4、双水解离子方程式的书写:
(1)左边写出水解的离子,右边写出水解产物;
(2)配平:在左边先配平电荷,再在右边配平其它原子;
(3)H、O不平则在那边加水。
例:当Na2CO3与AICI3溶液混和时:3CO32-
2AI3 3H2O = 2AI(OH)3↓ 3CO2个
5、写电解总反应方程式的方法:
(1)分析:反应物、生成物是什么;
(2)配平。
6、将一个化学反应方程式分写成二个电极反应的方法:
(1)按电子得失写出二个半反应式;
(2)再考虑反应时的环境(酸性或碱性);
(3)使二边的原子数、电荷数相等。
例:蓄电池内的反应为:Pb PbO2 2H2SO4=2PbSO4 2H2O 试写出作为原电池(放电)时的电极反应。
写出二个半反应:Pb-2e-→ PbSO4PbO2 2e-→ PbSO4
分析:在酸性环境中,补满其它原子,应为:
负极: Pb SO42--2e-= PbSO4
正极: PbO2 4H SO42- 2e-= PbSO4 2H2O
注意:当是充电时则是电解,电极反应则为以上电极反应的倒转:
阴极:PbSO4 2e-= Pb SO42-
阳极:PbSO4 2H20 -2e-= PbO2 4H SO42-
7、在解计算题中常用到的恒等:原子恒等、离子恒等、电子恒等、电荷恒等、电量恒等,用到的方法有:质量守恒、差量法、归一法、极限法、关系法、十字交法和估算法。
(非氧化还原反应:原子守恒、电荷平衡、物料平衡用得多,氧化还原反应:电子守恒用得多)
8、电子层结构相同的离子,核电荷数越多,离子半径越小;
9、晶体的熔点:原子晶体>离子晶体>分子晶体中
学学到的原子晶体有:Si、SiC、SiO2=和金刚石。
原子晶体的熔点的比较是以原子半径为依据金刚石> SiC> Si (因为原子半径:Si> C>O)。
10、分子晶体的熔、沸点:组成和结构相似的物质,分子量越大熔、沸点越高。
11、胶体的带电:一般说来,金属氢氧化物、金属氧化物的胶体粒子带正电,非金属氧化物、金属硫化物的胶体粒子带负电。
12、氧化性:MnO4->Cl2>Br2>Fe3 >12>S=4( 4价的S)
例:12 SO2 H2O = H2SO4 2HI
13、含有Fe3 的溶液一般呈酸性。
14、能形成氢键的物质:H2O 、NH3 、HF、CH3CH2OH 。
15、氨水(乙醇溶液一样)的密度小于1,浓度越大,密度越小,硫酸的密度大于1,浓度越大,密度越
大,98%的浓硫酸的密度为:1.84g/cm3。
16、离子是否共存:
(1)是否有沉淀生成、气体放出;
(2)是否有弱电解质生成;
(3)是否发生氧化还原反应;
(4)是否生成络离子[Fe(SCN)2、Fe(SCN)3、
Ag(NH3) 、[Cu(NH3)4]2 等];
17、地壳中:
含量最多的金属元素是— Al
含量最多的非金属元素是一O
HCIO4(高氯酸)—是最强的酸
18、熔点最低的金属是Hg (-38.9C。);
熔点最高的是W(钨3410c);
密度最小(常见)的是K;
密度最大(常见)是Pt。
19、雨水的PH值小于5.6时就成为了酸雨。
20、有机酸酸性的强弱:乙二酸>甲酸>苯甲酸>
乙酸>碳酸>苯酚>HCO3-
21、有机鉴别时,注意用到水和溴水这二种物质。
例:鉴别:乙酸乙酯(不溶于水,浮)、溴苯(不溶于水,沉)、乙醛(与水互溶),则可用水。
22、取代反应包括:卤代、硝化、礦化、卤代烃水解、酯的水解、酯化反应等;
23、最简式相同的有机物,不论以何种比例混合,只要混和物总质量一定,完全燃烧生成的CO2.
H2O及耗O2的量是不变的。恒等于单一成分该质量时产生的CO2、H2O和耗O2量。
24、可使溴水褪色的物质如下,但褪色的原因各自
不同:烯、炔等不饱和烃(加成褪色)、苯酚(取代褪色)、乙醇、醛、甲酸、草酸、葡萄糖等(发生氧化褪色)、有机溶剂[CCI4、氯仿、溴苯、CS2(密度大于水),烃、苯、苯的同系物、酯(密度小于水)]发生了萃取而褪色。
25、能发生银镜反应的有:醛、甲酸、甲酸盐、甲
酰铵(HCNH2O)、葡萄溏、果糖、麦芽糖,均可发生
银镜反应。(也可同Cu(OH)2反应)
计算时的关系式一般为:—CHO —— 2Ag
注意:当银氨溶液足量时,甲醛的氧化特殊:
HCHO —— 4Ag ↓ H2CO3
反应式为: HCHO 4[Ag(NH3)2]0H =
(NH4)2CO3 4Ag↓ 6NH3个 2H2O
,