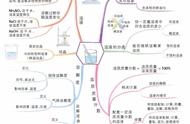
我们知道,溶质分散到溶剂里形成溶液的过程叫溶解。在溶解过程中,充满着复杂的变化,为帮助同学们理解物质的溶解过程,今就溶解过程中的“变”与“不变”作如下讨论:
一、溶解过程中的变化
1、温度变化。物质溶解到水里,通常发生两个过程:一是溶质微粒扩散的物理过程,这是吸收热量的;二是进入水中的溶质微粒与水化合的化学过程,这是放出热量的。这两个同时进行的过程中,由于吸热和放热的差值可能不同,使溶解过程中溶液的温度出现下列三种情形:
(1)吸收的热量大于放出的热量,溶解时表现为温度降低,如NH4NO3溶于水。
(2)吸收的热量约等于放出的热量,物质溶解时温度几乎不发生变化,如NaCl、KNO3等溶于水。
(3)吸收的热量小于放出的热量,物质溶解时表现为温度升高,如NaOH、H2SO4等溶于水。
2、颜色变化。物质在溶解时常伴随有颜色的变化。如:无水硫酸铜是白色的,将它溶于水却得到蓝色的溶液;高锰酸钾固体是紫黑色的,但将它溶于水却得到紫红色的溶液。
3、体积变化。物质溶解时也常伴随有体积的变化。如:将酒精与水混溶,溶液的总体积会小于酒精和水二者体积之和。其原因是由于分子间有间隔,溶质、溶剂分子相互溶入彼此的空隙中去了,故总体积减小了。
4、浓度变化。当溶液未饱和时,随着溶质的加入,溶液的浓度将不断地增大,这是不难理解的,因溶质的加入,使溶解的溶质在整个溶液中所占的比例不断地增加,所以,其浓度亦增大。
5、溶解速度变化。当溶质开始溶解的时候,溶剂中单位体积中的溶质分子数目较少,此时,溶解的速度较大,结晶速度较小;但随着溶解过程的进行,溶剂中的溶质分子数增多,由溶液里回到固体溶质表面的微粒也随之增加,溶解的速度逐渐减小,结晶速度逐渐增大,在形成饱和溶液时,溶解速度与结晶速度相等。
二、溶解过程中不发生变化的量
虽然在整个溶解过程中充满着极其复杂的变化,但有些量却在溶解时并不发生变化,尤其在溶液达到饱和时。如:
1、溶解度。当温度一定时,一种溶质在某种溶剂中的溶解度总是一定的,即只要温度一定,其溶解度就是不变的。
2、溶解速度与结晶速度。当溶液达到饱和时,在单位时间里,扩散到溶液里去的溶质微粒数目与回到固体溶质表面的溶质微粒数目相等,即溶解速度等于结晶的速度。
3、溶质质量。在饱和溶液中,由于溶解速度与结晶的速度相等,所以,在特定条件下,饱和溶液中的溶质质量是保持不变的。譬如:向饱和硫酸铜溶液中加入一定质量有缺损的胆矾晶体,一段时间后,其缺损部位即“自然修补”,成长为有规则形状的晶体了,但其质量仍与原晶体的质量相等。这一实验事实就是在饱和溶液中,溶质质量不发生变化的最好明证。
4、溶液浓度。由于溶液饱和以后,溶质的溶解和结晶速度相等,即进入溶剂的微粒等于从溶液中回到固体溶质表面的微粒数,使溶液中的溶质微粒数目不发生改变,所以,溶液的浓度也不变。
,