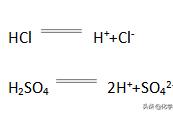2SO3 催化剂 Δ
59. 二氧化硫与硫化氢发生归中反应:
SO2 2H2S=3S↓ 2H2O (H2S臭鸡蛋气味)
60. 浓硫酸与铜加热发生反应:
2H2SO4(浓) Cu=CuSO4 SO2↑ 2H2O Δ
61. 浓硫酸与木炭加热发生反应:
2H2SO4(浓) C=2SO2↑ CO2↑ 2H2O Δ
62. 二氧化硫能使澄清石灰水变浑浊:
SO2 Ca(OH)2=CaSO3↓ H2O
63. 二氧化硫与氯气发生氧化还原反应:
SO2 Cl2 2H2O=H2SO4 2HCl
64. 酸雨的形成:
2SO2 O2

2SO3 粉尘等催化
SO3 H2O=H2SO4
SO2 H2O

H2SO3
2H2SO3 O2=2H2SO4
65. 海水提镁第一步:
Mg 2H =Mg2 H2↑ (盐酸、稀硫酸)
66. 镁与氮气的反应:
3Mg N2=Mg3N2 点燃
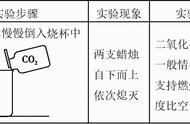
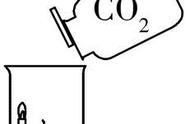
67. 镁与二氧化碳反应:
2Mg CO2=2MgO C 点燃 (镁着火不能用二氧化碳扑灭)
68. 海水提溴单质:
2Br- Cl2=Br2 2Cl-
69. 半导体硅与氧气的反应:
Si O2=SiO2 Δ(自然界没有游离态的硅)
70. 工业上制粗硅:
SiO2 2C=Si 2CO↑ 高温 (光导纤维、沙子和石英的主要成分是SiO2)
71. 硅与氟气的反应:
Si 2F2=SiF4
72. 硅与氢氟酸的反应:
Si 4HF=SiF4 2H2
73. 制作黏合剂:
Si 2NaOH H2O=Na2SiO3 2H2↑
74. 玻璃与烧碱反应:
SiO2 2NaOH=Na2SiO3 H2O (Na2SiO3的水溶液称为水玻璃)
75. 二氧化硅与碱性氧化物的反应:
SiO2 CaO=CaSiO3 高温
76. 刻蚀玻璃:
SiO2 4HF=SiF4↑ 2H2O
77. 工业制玻璃:
CaCO3 SiO2=CaSiO3 CO2↑ 高温
Na2CO3 SiO2=Na2SiO3 CO2↑ 高温
78. 金属铝在氧气中燃烧:
4Al 3O2=2Al2O3 点燃
79. 铝热反应:
2Al Fe2O3=Al2O3 2Fe高温
(铝粉与氧化铁粉的混合物称为铝热剂,用于焊接钢轨)
80. 金属铝与酸的反应:
2Al 6HCl=2AlCl3 3H2↑
81. 金属铝与碱的反应:
2Al 2NaOH 6H2O=2Na[Al(OH)4] 3H2↑ (四羟基合铝酸钠)
82. 实验室制氢氧化铝:
AlCl3 3NH3·H2O=Al(OH)3↓ 3NH4Cl(白色沉淀)
83. 氢氧化铝溶于强酸中:
Al(OH)3 3H =Al3 3H2O
84. 氢氧化铝溶于强碱中:
Al(OH)3 OH-=[Al(OH)4]- (四羟基合铝酸根离子)
85. 氧化铝溶于强酸:
Al2O3 6H =2Al3 3H2O (氧化铝为两性氧化物)
86. 氧化铝溶于强碱:
Al2O3 2OH- 3H2O=2[Al(OH)4]-
87. 碱式碳酸铜的制取:
2Cu O2 H2O CO2=Cu2(OH)2CO3 (绿色)
88. 铜与氧气的反应:
Cu O2=2CuO Δ
89. 铜与硫粉的反应:
2Cu S=Cu2S Δ
90. 4CuO=2Cu2O O2↑ 高温 (黑色物质变为红色物质)
91. CuSO4·5H2O=CuSO4 5H2O↑ Δ (蓝色晶体变为白色粉末)
92. 氯化铝与少量的氢氧化钠反应:
Al3 3OH-=Al(OH)3↓
93. 氯化铝与过量的氢氧化钠反应:
Al3 4OH-=[Al(OH)4]-
94. 四羟基合铝酸根离子与酸的反应:
[Al(OH)4]- H =H2O Al(OH)3↓
95. 实验室制取氯气:
4HCl(浓) MnO2 =MnCl2 Cl2↑ 2H2O Δ (黄绿色气体、有毒、密度比空气大)
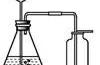
96. 实验室制取二氧化碳:
CaCO3+2HCl=CaCl2 H2O CO2↑ (无色无味、密度比空气大,溶于水)

不过小编认为,本文只适合查缺补漏,巩固你方程式的掌握情况和熟练程度,化学方程式有很多巧妙的方法,一定要背,但不能死记硬背,大家一定要注意哦,特别是氧化还原反应,只要能够抓住常见氧化剂还原剂及对应产物的关系,基本不用背诵。
▐ 标签:高考化学 化学方程式
▐ 更多内容请关注微信公众号平台:高考化学 ID:gkhx100
,