今天给大家整理了高中化学300个知识盲点汇总!!看看你都掌握了哪些?

1、钝化现象:铁、铝在冷的浓硝酸或浓硫酸中钝化。钝化只在常温下用,加热条件下铁会与浓硫酸反应。
2Fe 6H2SO4(浓)=Fe2(SO4)3 3SO2↑ 6H2O 钝化是指活泼金属在强酸中氧化表面生成一层致密的氧化膜组织金属进一步反应。
2、浓盐酸、浓硝酸,在离子方程式中拆开,浓硫酸不拆开。
3、在离子方程式中,澄清石灰水要拆开写成离子,浑浊石灰乳不拆。
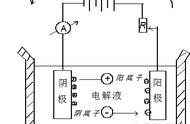
4、有阴离子必有阳离子,有阳离子未必有阴离子,如金属中只有自由电子。
5、氢氧化钠与乙醇不反应。
6、阿伏伽德罗常数考点陷阱有:未告知体积,如PH=1的盐酸溶液中,氢离子的个数为0.1NA。
7、苯中无C=C双键。
8、碳酸钠俗名是纯碱、苏打,显碱性但不是碱,是盐。(稳定)
9、小苏打是碳酸氢钠,加热分解成碳酸钠、二氧化碳和水。(不稳定)在推断题中会出。
10、醋酸、苯酚、水、乙醇,分子中羟基上氢原子的活泼性依次减弱。故,氢氧化钠与乙醇不反应。

11、碱金属元素的熔沸点是原子半径越大熔沸点越低;卤素单质是分子晶体,靠范德华力结合,范德华力大小与分子量有关,分子量越大范德华力越大,熔沸点也就越高。碱金属元素是金属晶体,结合键是金属键,原子半径越小原子核间的引力越强,越难破坏,熔沸点越高。#随着核电荷数的递增,熔沸点逐渐降低(与卤素、氧族相反)
12、锂与氧气反应只生成氧化锂,钠在常温生产氧化钠,加热或完全燃烧生成过氧化钠。
13、碱金属的特殊性:锂的密度比煤油小,不能保存在煤油中,通常密封在石蜡里,钠的密度比水小,比煤油大。
14、碱金属的密度由锂到铯逐渐增大的趋势,但是有反常的钠密度比钾的大。
15、酸式盐的溶解度一般比相应的正盐大,但是碳酸钠比碳酸氢钠的溶解度大。
16、煤的干馏是化学变化,蒸馏和分馏是物理变化。
17、蛋白质的变性是化学变化,盐析是物理变化。
18、碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物。Mn2O7是金属氧化物,但它是酸氧化物,其对应的酸是高锰酸,即HMnO4。
19、酸性氧化物不一定是非金属氧化物(如Mn2O7),非金属氧化物也不一定是酸性氧化物(如H2O、CO、NO)。
20、酸性氧化物大多数能溶于水并与水反应生成对应的酸,记住二氧化硅(SiO2)不溶于水。碱性氧化物的概念:能跟酸起反应,生成盐和水,且生成物只能有盐和水。
21、氧化性:Cl2>Br2>Fe3 >I2>S;还原性:碘离子>亚铁离子>溴离子>氯离子
22、22.4L,一定是标况下,气体,四氯化碳、苯、水、酒精、三氧化硫、碳原子数大于4的烃(新戊烷在标况下是气体)都不是气体,且记得混合时是否反应比如NO和O2。
23、次氯酸是弱电解质,离子方程式不拆开。
24、随着反应的进行,浓会逐渐变稀,故不能进行到底,比如二氧化锰与浓盐酸反应。
25、水玻璃为硅酸钠等易容性硅酸盐的混合物。
26、银氨溶液配制方法:在AgNO3溶液中加入稀氨水
AgNO3 NH3.H2O = AgOH↓ NH4NO3
接着加稀氨水:AgOH 2NH3.H2O =Ag(NH3)2 OH 2H2O ,到沉淀刚好溶解停止.
27、偏铝酸根与氢离子反应:如果是H 少量发生 H H2O AlO2-=Al(OH)3 ↓ 如果是大量H 那么 AlO2- 4H =Al3 2H2O
28、泡沫灭火器的反应原理:双水解的应用:Al2(SO4)3 6NaHCO3==3Na2SO4 2Al(OH)3↓ 6CO2↑
29、苯酚钠与二氧化碳,无论二氧化碳通过多少,只生产碳酸氢钠,C6H5ONa CO2 H2O==C6H5OH NaHCO3。
30、苯酚才能与碳酸钠反应:
C6H5-OH Na2CO3 --→ C6H5-ONa NaHCO3
这个反应能发生,是因为苯酚酸性强于碳酸氢根。苯酚钠只能与二氧化碳反应:
C6H5-ONa CO2 H2O --→ C6H5-OH NaHCO3
该反应能发生,因为碳酸酸性强于苯酚。

31、磷与氯气反应,氯气充足生成五氯化磷,氯气不足生成三氯化磷。
32、白磷分子式为P4、分子晶体,故12.4g白磷含有磷原子数目为0.4NA。
33、Cl2与足量Fe反应,无论铁过量还是未过量,只生成氯化铁,只有溶液中铁才与氯化铁反应生产氯化亚铁。
34、Al3 3 AlO2- 6 H2O =4 Al(OH)3↓
35、过量二氧化碳通入水玻璃中反应为:
2H2O 2CO2 Na2SiO3=2NaHCO3 H2SiO3↓,二氧化碳不过量生成碳酸钠。
36、比较半径大小:(1)层数相同,核大半径小(2)层异,层大半径大(3)核同,价高半径小,例如铁大于二价铁大于三价铁(4)电子层结构相同,核电荷数越大,半径越小。
37、C是形成化合物最多的元素、单质是自然界中硬度最大的物质元素或气态氢化物中氢的质量分数最高的元素。
38、元素气态氢化物能和它的氧化物在常温下反应生成该元素单质的是S。这是高中很重要的化学反应,也是唯一体现二氧化硫具有氧化性的反应。2H2S SO2=2H2O 3S
39、元素的气态氢化物和它的最高价氧化物对应的水化物能反应生成盐的元素为N。
40、单质在常温下呈液态的非金属元素为Br.单质在常温下呈液态的金属元素为:Hg。