第七章 应用广泛的酸碱盐

第一节:溶液的酸碱性
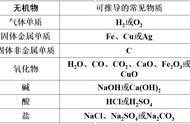
一. 物质分类
二. 溶液的酸碱性
1. 检验方法:①酸碱指示剂 (紫色)石蕊试剂: 酸红碱蓝
(无色) 酚酞 :酸不变色碱变红
②石蕊试纸 红色石蕊试纸:检验碱
蓝色石蕊试纸:检验酸
2. 酸性:酸的溶液(某些盐) eg.H2SO4 (盐:CuSO4) 家庭: 醋 果
汁 洁厕灵 碳酸饮料等
碱性:碱的溶液(某些盐) eg.NaOH Ca(OH)2 家庭 :肥皂水
洗涤剂 石灰水 草木灰
中性:大多数的溶液 eg. NaCl溶液 水 蔗糖水 等等

三.溶液的酸碱度(用 PH 表示)
1. 测量方法: ①PH 试纸 与标准比色卡进行对比
步骤:用玻璃棒蘸取待测液,滴在 PH 试纸上,与标准的比色
卡进行对比,测得的数值为 PH 值 (只取整数 )
②PH 计
3.PH值:0—14
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
↓
酸性增强 中性 碱性越强
eg. 酸雨 PH<5.6 (很重要) 胃酸<1.5
3. PH 的应用:
改良酸性土壤 : 用熟石灰(生石灰)

第二节、常见的酸
一.常见的酸
1、浓盐酸(HCI) :
物性:无色有刺激性气味、易挥发的液体(打开瓶盖在空气中形成白雾、质量减
轻、质量分数减小);
用途:除锈、制药、胃酸帮助消化等。
2、浓硫酸(H2SO4) :
物性:无色无味、粘稠油状液体,不易挥发,具有吸水性(打开瓶盖,能
吸收空气中的水蒸气、质量增加、浓度减小)。
腐蚀性(脱水性): 夺取物质中的水分,生成黑色的碳。黑面包实验
用途:作干燥剂;制化肥、药等;金属除锈
稀释:一定要把浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断搅拌(加速散热)。
切不可将水倒进浓硫酸里。(重中之重)
3.硝酸
无色刺激性气味的液体,有挥发性,有白雾,见光易分解,装在棕色的试剂瓶中
二、酸的通性(酸的化学性质)
1.能使酸碱指示剂显不同的颜色。 (石蕊遇酸变红色,酚酞遇酸不变色)
2.和活泼金属(H前金属)反应,生成盐和 H2.
铁和硫酸溶液反应: Fe H2SO4 === FeSO4 H2↑
铁和盐酸的反应 : Fe 2HCl=== FeCl2 H2↑
锌和稀硫酸反应(实验室制氢气): Zn H2SO4 === ZnSO4 H2↑
铝和稀盐酸 : 2Al 6HCl =2AlCl3 3 H2↑
镁和稀盐酸反应: Mg 2HCl === MgCl2 H2↑
金属活动顺序表 嫁给那美女 K Ca Na Mg Al
身体细纤氢 Zn Fe Sn Pb H
统共一百斤 Cu Hg Ag Pt Au
越靠前与酸反映的越剧烈