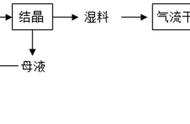
①加快反应速率
研磨:减小固体的颗粒度,增大固体与液体或气体间的接触面积,加快反应速率。
②溶解:通常用酸溶,如用硫酸、盐酸、浓硫酸等
水浸:与水接触反应或溶解
浸出:固体加水(酸)溶解得到离子
浸出率:固体溶解后,离子在溶液中含量的多少(更多转化)
酸浸:在酸溶液中反应使可溶性金属离子进入溶液,不溶物通过过滤除去的溶解过程
③灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质高温下氧化、分解
④控制反应条件的方法
如控制温度,根据需要升温或降温,改变反应速率或使平衡向需要的方向移动。

①调pH值除杂
a.控制溶液的酸碱性使其中某些金属离子形成氢氧化物沉淀
例如:已知下列物质开始沉淀和沉淀完全时的pH如下表所示
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
若要除去Mn2+溶液中含有的Fe2+,应该怎样做?
提示:先用氧化剂把Fe2+氧化为Fe3+,再调溶液的pH到3.7。
b.调节pH所需的物质一般应满足两点:
能与H+反应,使溶液pH值增大;
不引入新杂质。
例如:若要除去Cu2+溶液中混有的Fe3+,可加入CuO、Cu(OH)2、Cu2(OH)2CO3等物质来调节溶液的pH值。
②试剂除杂
a.趁热过滤。防止某物质降温时会析出。
b.冰水洗涤。洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗。
③加热:加快反应速率或促进平衡向某个方向移动
如果在制备过程中出现一些受热易分解的物质或产物,则要注意对温度的控制。
如:侯氏制碱中的NaHCO3;还有如H2O2、Ca(HCO3)2、KMnO4、AgNO3、HNO3(浓)等物质。
④降温:防止某物质在高温时会溶解(或分解)、为使化学平衡向着题目要求的方向移动
⑤萃取
,