问题剖析:化合价变化本质的原因分析
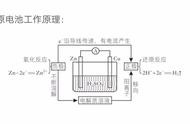
化合价升降本质原因——电子的得失
化合价升降的本质原因——共用电子对的偏移
氧化还原反应中电子转移的表示方法
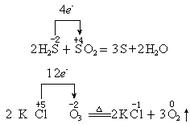
1.双线桥表示法
表明同种元素反应前后的电子转移情况。双线桥法的基本步骤:
(1)正确标出变价元素的化合价,判断其升降。
(2)一条线由还原剂化合价升高的元素指向氧化产物中对应的元素,另一条线由氧化剂化合价降低的元素指向还原产物中对应的元素。
(3)在线上标出失去或得到电子的数目,注明该元素被氧化还是被还原。
注意事项
(1)箭头必须由反应物指向生成物中的同种元素。
(2)在“桥”上标明电子“得到”与“失去”,且得到与失去的电子总数必须相等。
(3)采用“a×be-”形式表示得失电子数,a为得失电子的原子总数,b为每个原子得失电子数,当a或b是“1”时省略“1”。
2.单线桥法
表明反应中不同元素原子间的电子转移情况。
单线桥法的基本步骤
(1)正确标出变价元素的化合价,判断其升降,确定电子转移数目。
(2)箭头从还原剂中元素化合价升高的元素指向氧化剂中元素化合价降低的元素。
(3)在线上标出电子转移的总数。
注意事项
(1)单线桥从还原剂中失电子的元素指向氧化剂中得电子的元素,表示氧化剂和还原剂中变价元素原子间电子的转移情况。
(2)箭头已标明电子转移的方向,因此不需再标明“得”或“失”,只标明电子转移数目。
氧化还原反应必然存在着对立统一的关系:元素化合价有升必有降,电子有失必有得,有氧化必有还原,氧化和还原同时存在,同时消失。我们表示氧化还原反应中与电子转移、化合价升降、物质被氧化、被还原等关系时,用双线桥法比较具体直观;如果表示电子转移的方向和数目时,用单线桥法较简洁方便。



,