在测量工具和测量方法缺乏的十八世纪,拉瓦锡善于充分利用天平的作用对空气组成成分进行了详实的定量研究,从而建立了燃烧的氧学说。

拉瓦锡(A. -L. Lavoisier,1743-1794)
拉瓦锡是如何定量测定空气中氧气含量的?1773年,31岁的拉瓦锡在《物理化学简论》中指出:在钟罩里的水银(Hg)面上燃烧白磷(P4),燃烧后水银面上升,表明部分空气被消耗,剩下的空气不能使白磷燃烧;1盎司的白磷大约可得到2.3盎司的五氧化二磷白色粉末(P2O5,当时其化学式未知),其增加的重量和所消耗的五分之一容积的空气质量几乎相等。
那么,为什么拉瓦锡又用汞来定量研究空气的成分呢?
当时受燃素学说的影响,当时空气的组成成分仍然是迷。1775年,法国化学家贝岩在《物理学报》中描述了“红色沉淀物”(氧化汞,HgO)热分解实验:在未加任何含有燃素的物质条件下,氧化汞受热生成金属汞,质量减少了十五分之一,同时放出大量气体。但是他并没有将气体收集起来进行深入研究。

拉瓦锡研究空气成分所用的装置
受此启发,1777年,拉瓦锡在一个大曲颈甑(A)加热水银,甑与钟罩(E)内水银面上的空气相通,连续加热十二天,容器中气体体积减少了将近五分之一,部分银白色的汞变成了红色的氧化汞粉末。他又研究了剩下的五分之四体积的气体,发现这部分剩余的气体既不能供给呼吸,又不支持燃烧。
拉瓦锡将红色粉末收集起来重复贝岩的实验,他将放出的气体收集起来,并和上面的剩余气体混合起来再次组成了通常的空气。由此,他抨击了错误的燃素学说,建立了燃烧的氧学说。

汞与氧气加热反应及氧化汞加热分解化学方程式
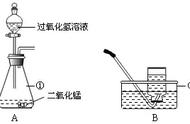
教科书上测定空气中氧气含量的实验用汞来测定空气中氧气的含量有以下几个缺点:1)汞蒸汽有毒;2)耗时长,需要连续加热12天;3)耗能大;又由于白磷能自燃,比较危险,因而教科书上普遍使用红磷(P)来代替白磷进行氧气含量测定的实验。