81.关于各种“谱”(研究工具)
原子光谱:鉴定元素
质谱:得知相对分子质量
红外光谱:得知化学键和官能团
核磁共振氢谱:得知有几种化学环境相等的氢
X射线衍射:得知更细致的数据(键长、键角……),主要用于晶体
82.关于各种“式”
实验式:最简比!苯的实验式是CH
分子式:首先必须是分子,其次每种元素合并写
(C2H6O是分子式,CH3CH2OH不是)
化学式:离子晶体、分子晶体、原子晶体、金属晶体都能用
83.关于各种模型
球棍模型:有球有棍!教材有时也说“分子结构模型”
空间填充模型:像泡泡一样粘在一起
84.关于同系物
同分异构体不是同系物!
官能团相同是同系物的必要条件:
1-丁烯和环戊烷不是同系物;
1,3-丁二烯和丙炔不是同系物;
官能团相同也不一定是同系物:苯酚和苯甲醇官能团都是羟基,但前者属于
酚,后者属于醇,不是同系物!
85.关于命名
选主链:最长
标号:最小
阿拉伯数字:基团位置
汉字数字:基团有几个
另:“二乙酯”和“乙二酯”的区别:命名之时“醇”换“酯”
86.有机物的密度
在水上层:乙酸乙酯、苯、油脂
在水下层:溴乙烷、四氯化碳
87.苯的卤代
实验时:加入的是铁粉和液溴(不是溴的水/四氯化碳溶液)
实际:起催化作用的是FeBr3
(以溴代为例)
88.苯和取代苯反应的区别
苯:
溴代:必须溴单质,需要催化剂,速率慢;
硝化:生成单取代产物
苯酚:
溴代:溴水就可以,不需催化剂,立刻反应;
甲苯:
硝化:生成三取代产物
体现了:甲基(不是官能团!)和羟基对苯环的活化
89.苯酚的性质
酸性:H2CO3>苯酚>HCO3-,苯酚钠不能和碳酸共存,苯酚不能和碳酸根共存;
可和碳酸钠反应(不生成CO2),和NaOH反应,和Na反应
溶解性:微溶于水,65℃以上与水混溶
体现了:苯环对羟基的活化
90.银镜反应
滴加顺序:向硝酸银溶液中滴加氨水
现象:先沉淀再溶解
产物:乙酸铵、银
可发生银镜反应的物质:醛、甲酸
做完实验之后:用浓硝酸洗掉银镜
91.溴水检验官能团的特例——和醛基反应
92.陌生有机物与NaOH反应的特例
酚羟基、碳卤键、酯基、酰胺基都可以和NaOH反应
特例:一般的酯基碱性条件下水解,1mol酯基消耗1molNaOH;
苯酚形成的酯基,1mol消耗2molNaOH
93.高分子材料的生活应用
塑料:
聚乙烯(做包装袋等),是“热塑性”的,可以反复熔融加工;是加聚反应
的产物;
聚氯乙烯加热分解产生有毒物质,不能用于食品包装
酚醛树脂(做绝缘、隔热、阻燃、复合材料),是“热固性”的,只能一次
成型;是缩聚反应的产物。
合成纤维:与“天然纤维”(棉花等)对应,包括聚酯、聚酰胺等等
合成橡胶:与“天然橡胶”对应,如顺丁橡胶(1,4-加成的产物)
可降解高分子:如聚乳酸
“新型”:如聚丙烯酸钠,吸水性强,可做“尿不湿”
*不粘锅是聚四氟乙烯
94.煤和石油的综合利用
煤:
干馏:化学变化,隔绝空气加强热,得焦炭、煤焦油和煤气等
气化:化学变化,转化为CO、H2
等
液化:化学变化,“煤制油”,转化为液态的烃
石油:
分馏:物理变化,相当于蒸馏,得汽油、煤油、柴油、沥青等
裂解/裂化:化学变化,将长链烃变为短链烃
催化重整:化学变化,链状烃转化为环状烃,芳香烃的重要来源
*“水煤气”是水蒸气高温下通过焦炭得到的气体,主要是CO和H2的混合气
95.生活中常见的一些有机化合物
味精:谷氨酸钠
食品防腐剂:苯甲酸钠、山梨酸钾)、*亚硝酸钠(不是完全不能加,可以按标准加一点点)
抗氧化剂:维生素C(具有还原性!水溶液中或受热容易被氧化)
阿司匹林:乙酰水杨酸(邻羟基苯甲酸乙酯)
*关于维生素:
脂溶性:A、D、E、K;
水溶性:C、B族
96.关于糖类
单糖:葡萄糖能发生银镜反应、与氢氧化铜反应,属于醛糖;
果糖属于酮糖;
单糖都不能发生水解反应;
二糖:蔗糖=葡萄糖 果糖,不是还原糖
麦芽糖=2×葡萄糖,是还原糖
都可以水解(酸性环境或酶)
多糖:淀粉和纤维素都是葡萄糖单元相互连接而成
淀粉和纤维素不是同分异构体!
都属于非还原糖,都可以水解(酸性环境或酶)
97.关于油脂
油脂:高级脂肪酸与甘油(丙三醇)形成的酯
饱和脂肪酸:脂肪酸的碳链是烷基链
不饱和脂肪酸:碳链上有双键(可以氢化加成掉)
液态是“油”,固态是“脂”
油酸是不饱和脂肪酸(C17H33COOH),硬脂酸是饱和脂肪酸
(C17H35COOH)
油脂在碱性条件下的水解反应又称为皂化反应;
油脂可以催化加氢(“氢化植物油”)由液态变为半固态(人造奶油)
98.关于蛋白质
氨基酸具有两性:能和酸、碱反应生成盐
两种氨基酸可以形成4种二肽,不同二肽可以得相同的水解产物
水解:条件为酸、碱或酶
盐析:某些盐(不是重金属盐,如硫酸钠、硫酸铵、氯化钠)能促进蛋白质溶解,
盐浓度增大到一定程度时,蛋白质溶解度又降低从而析出是可逆过程,不影响活性
变性:重金属盐(如硫酸铅)、强酸碱、甲醛、乙醇、加热、射线、…不可逆,影响活性
(误服重金属盐溶液,应服用大量牛奶)
显色:含有苯环的蛋白质与浓硝酸生成白色沉淀,加热后变黄色
鉴别:灼烧,有烧焦羽毛气味
99.关于氨基酸的存在形式

100.核酸
教材出处:部编选修3 P119、鲁科选修3P83
描述:
磷酸、戊糖和碱基通过一定方式结合而成的生物大分子
101.生物大分子
淀粉、纤维素、蛋白质、核酸是生物大分子,也属于高分子
脂肪不是生物大分子,更不是高分子
*棉麻(植物)主要是纤维素(C、H、O),丝绸羊毛头发(动物)主要是蛋
白质(C、H、O、N、S)
第六节 化学实验
102.常见易错仪器名称
容量瓶 坩埚(注意偏旁) 坩埚钳 长颈漏斗 分液漏斗
蒸发皿 干燥管 蒸馏烧瓶 三脚架 泥三角(不是三脚架)
表面皿(和蒸发皿区分) 球形冷凝管 直形冷凝管 三颈烧瓶
圆底烧瓶 锥形瓶 烧杯 胶头滴管 试管夹
45:15 · 不方便截图,自己点传送门
103.配制溶液
一定质量分数的溶液:不用容量瓶,用量筒和天平
一定物质的量浓度的溶液:用容量瓶、天平、烧杯、玻璃棒、胶头滴管
先在烧杯中溶解,然后转移(玻璃棒引流)
蒸馏水洗涤烧杯和玻璃棒两到三次,洗涤液也转移(防止损耗)
最后定容时用胶头滴管滴加
定容之后才能盖盖,然后上下颠倒摇匀
容量瓶不能加热!
104.物质检验时的注意事项
用BaCl2
检验硫酸根:排除SO32-、Ag 的影响(先用盐酸酸化,探路);
用AgNO3
检验氯离子:排除CO3
2-的影响(先用硝酸酸化); ……
体系中有HCl时,不能用KMnO4
检验还原性微粒; ……
Ca(OH)2不能区分NaHCO3和Na2CO3
105.无机化学制备实验中的洗气
制备氯气:洗HCl,用饱和食盐水;
制备SO2:洗硫酸酸雾,用饱和NaHSO3
溶液;
制备CO2:洗盐酸(挥发),用饱和NaHCO3
溶液
106.课内有机化学实验中的注意事项
用乙醇制备乙烯:杂质主要是乙醇、二氧化硫
温度计伸到液体中,量程要大于170℃
用溴乙烷制备乙烯:杂质主要是溴化氢(用水洗)
用电石制备乙炔:杂质主要是硫化氢、磷化氢,用硫酸铜溶液洗
用饱和食盐水反应,控制反应速率
酯化反应:用饱和Na2CO3溶液吸收,导管不伸入
107.课内探究实验中的注意事项
排除溶液挥发性的干扰:右图
加少量还是加过量:沉淀溶解平衡的探究
控制变量:一组加试剂,另一组加蒸馏水;
FeCl3和Fe2(SO4)3
在同一个实验中应用,要注意什么?
选择恰当的变量:用酸性高锰酸钾和草酸的反应探究浓度
对反应速率的影响,控制谁的浓度不变?(高锰酸钾,不然褪色速度无可比性)
排除干扰:密切关注NO3-等离子(氧化性干扰)
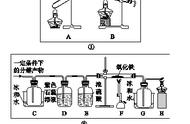
108.防倒吸装置
使用场合:水中溶解度很大的气体(如NH3)
第一种:用漏斗
第二种:用密度比水大的有机溶剂
(个人刷到过使用干燥管防倒吸的题目)