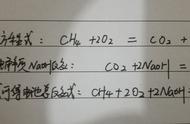40电极反应式的书写知识点
原电池电极反应式的书写方法
1.负极反应式的书写
先判断负极材料,然后再分析其反应特点,并注意电解质溶液的成分对电极产物的影响。
2.正极反应式的书写
(1)首先判断在正极发生反应的物质
①当负极材料与电解质溶液能自发的发生氧化反应时,在正极上发生电极反应的物质是电解质溶液中的某种微粒;
②当负极材料与电解质溶液不能自发的发生氧化反应时,在正极上发生电极反应的物质是溶解在电解质溶液中的O2。
(2)然后再根据具体情况写出正极反应式,在书写时也要考虑正极反应产物是否与电解质溶液反应的问题,若参与反应要叠加在一起书写。
(3)甲烷燃料电池用铂作电极插入KOH溶液中,其正极反应式是O2+2H2O+4e-=4OH-;铜锌原电池(Zn-Cu-H2SO4)的正极反应式是2H++2e-=H2↑。
原电池中电极反应式的书写时注意的问题
(1)如果题目给定的是图示装置,先分析正、负极,再根据正、负极反应规律写电极反应式。
(2)确认电极得失电子后的产物是否与电解质溶液发生反应,若能反应,则应写与电解质溶液反应后的电极反应式。
(3)在正极上,若是电解质溶液中的某种离子被还原,提供该离子的电解质无论电离难易如何,一律写离子符号(而在原电池反应中,要遵循离子方程式的书写规则,只有易溶的强电解质用离子符号表示)。
(4)如果题目给定的是总反应式,可分析此反应中的氧化反应或还原反应(即分析有关元素化合价的变化情况),再选择一个简单变化情况写电极反应式,另一极的电极反应式可直接写或将各反应式看作数学中的代数式,用总反应式减去已写出的电极反应式即得结果。
(5)需要特别指出,对于可逆电池的反应,需要看清楚"充电"、"放电"的方向,放电的过程应用原电池原理,充电的过程应用电解原理。
电解时两电极产物的判断与电极反应式的书写
1.阳极产物的判断
(1)活性金属电极(金属活动性顺序表中排在Ag之前),电极金属失电子,生成对应的金属阳离子,阴离子不放电。
(2) 惰性电极(Au、Pt、石墨),溶液中的阴离子失电子,生成对应的非金属单质或高价化合物。
阴离子放电顺序:S2->I->Br->Cl->OH->高价态含氧酸根>F-。
2.阴极产物的判断
与电极材料无关,直接根据阳离子放电顺序进行判断,溶液中的阳离子得电子生成对应的单质或低价化合物。阳离子的放电顺序:Ag+>Hg2+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Ni2+>Fe2+>Zn2+>Mn2+>较活泼金属阳离子(注意Fe3+的顺序)。
3.电极反应式与电解反应式的书写(以石墨电极电解CuCl2溶液为例)
(1)电极反应式的书写
①确定阴、阳极。与电源正极相连的为阳极、与电源负极相连的是阴极。②分别写出两极上出现的离子。阴极:Cu2+、H+,阳极:Cl-、OH-。③判断阴、阳极放电顺序。阴极:Cu2+>H+,阳极: Cl->OH-。④写电极反应式。列物质→标得失→选离子、配电荷→配原子个数
阴极:Cu2++2e-===Cu,阳极:2Cl--2e-===Cl2↑
(2)电解反应方程式的书写
①通过最小公倍数法使两个电极反应式的电子数相等。
②把两个电极反应式相加,消去相同项,并注明条件"通电"。
电解CuCl2溶液总反应方程式为:CuCl2=(通电))Cu+Cl2↑
,