【分析】Ⅰ.(1)根据常见仪器的名称进行分析;
(2)根据二氧化碳和水反应生成碳酸进行分析;
(3)根据二氧化碳的检验方法进行分析;
【设计并完成实验】根据氢氧化钙和氯化铜的反应及碳酸钙和稀盐酸的反应进行分析;
【实验结论】根据实验现象进行分析;
【交流与反思】根据氢氧化钙的检验及氧化钙和水的反应进行分析;
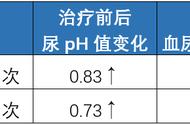
【拓展与分析】根据表中数据进行分析。
【解答】解:Ⅰ.(1)仪器a是锥形瓶,故答案为:锥形瓶;
(2)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊溶液变红色,故答案为:石蕊试液变红色;
(3)生成的气体是二氧化碳,检验二氧化碳利用澄清石灰水,反应的方程式为CO2 Ca(OH)2=CaCO3↓ H2O,故答案为:澄清石灰水;CO2 Ca(OH)2=CaCO3↓ H2O;
【设计并完成实验】上层清液中一定含有氢氧化钙,加入氯化铜后,氯化铜和氢氧化钙反应生成氢氧化铜蓝色沉淀和氯化钙,现象是有蓝色沉淀产生,部分底部白色不溶物于第三支试管中,滴加过量稀盐酸,有气泡产生,说明有碳酸钙存在,故答案为:有蓝色沉淀产生;碳酸钙;
【实验结论】根据上述实验得出固体中含有碳酸钙,溶液中含有氢氧化钙,则固体中含有氧化钙,则猜想二成立,故答案为:猜想二;
【交流与反思】溶液中只有氢氧化钙是碱性的,因此还可以选择无色酚酞溶液,滴加无色酚酞溶液,溶液变红色,则含有氢氧化钙,小华同学认为,只需完成步骤一和步骤三即可获得相同实验结论,他的依据是氧化钙和水反应放热,温度升高,即可知道剩余固体中有氧化钙,故答案为:无色酚酞溶液;氧化钙和水反应放热,温度升高,即可知道剩余固体中有氧化钙;
【拓展与分析】由表中水可知,燃烧时间长短不同,在1100℃~1200℃范围内生石灰的活性度均高,故答案为:燃烧时间长短不同,在1100℃~1200℃范围内生石灰的活性度均高。
【点评】本题主要考查学生根据物质的性质分析物质成分的能力,有一定难度。
三、计算题(4分)
14.(4分)碳酸氢钠是发酵粉的主要成分,常用作糕点、馒头的发泡剂。为测定某碳酸氢钠样品中NaHCO3的质量分数,称取20.0g样品,加热至恒重(质量不再变化),称得固体质量为13.8g。(已知:样品中杂质在加热过程中不发生变化)
(1)计算样品中NaHCO3的质量分数。(写出计算过程)
(2)若上述测定过程中未加热至恒重,则测得NaHCO3的质量分数将 偏小 。(填“偏小”、“偏大”或“无影响”)。
【分析】根据质量守恒定律,混合物减少的质量即为生成二氧化碳和水的质量之和,由反应的化学方程式列式计算出参加反应的碳酸氢钠的质量即可。
【解答】解:(1)生成二氧化碳和水的质量之和为20g﹣13.8g=6.2g。
设样品中NaHCO3的质量为x。
2NaHCO3

Na2CO3 H2O CO2↑
168 18 44 18 44=62
x 6.2g

x=16.8g
样品中NaHCO3的质量分数为

×100%=84%。
(2)若上述测定过程中未加热至恒重,测定的剩余固体的质量偏大,则测得NaHCO3的质量分数将偏小。
答:(1)样品中NaHCO3的质量分数为84%。
(2)偏小。
【点评】本题有一定难度,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳和水的质量之和是正确解答本题的前提和关键。
,