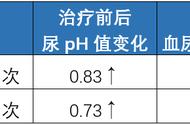
2CO2 (写其中一个即可)。
(3)下列说法正确的是 AD (填字母标号)。
A.能源结构向多元、清洁、低碳转型
B.太阳能属于不可再生能源
C.生活中的废热无法利用
D.化学与新能源开发密切相关
【分析】(1)根据图一进行分析;
(2)根据通过光催化得到太阳能燃料,该过程是将光能转化为化学能能;根据资料中的信息,在太阳光照下,通过光依化将H2O、CO2直接转化为CH3OH、H2、CO、CH4等太阳能燃料分析;
(3)根据资料进行分析。
【解答】解:(1)从图一可以看出,转化过程中循环利用的物质有Fe3O4和FeO;与电解水相比,该方法是在太阳能作用下将水分解生成氢气和氧气,故其优点是能耗低;故答案为:能耗低;
(2)通过光催化得到太阳能燃料,该过程是将光能转化为化学能能;根据资料中的信息,在太阳光照下,通过光依化将H2O、CO2直接转化为CH3OH、H2、CO、CH4等太阳能燃料,燃烧的化学方程式可以为:2CO O2

2CO2;故答案为:2CO O2

2CO2(合理即可)。
(3)A、能源结构向多元、清洁、低碳转型,正确;
B、太阳能属于可再生能源,错误;
C、生活中的废热无法利用,错误;
D、化学与新能源开发密切相关,正确;
故选:AD。
【点评】此题考查知识点较多,可依据已有的知识进行解答。能读懂题意,从原题情景中提炼出有用的信息是解决该题的关键。
12.(5分)回收含铜废料(主要成分为Cu)中的铜,部分实验流程如下:

注:灼烧后得到黑色固体和残留物,残留物不溶于水和稀硫酸。
回答下列问题:
(1)“灼烧”的主要目的是 将Cu转化为CuO 。
(2)“酸溶”发生反应的化学方程式为 CuO H2SO4=CuSO4 H2O ,反应类型为 复分解反应 。
(3)“转化”生成气体X的成分为 氢气(或H2) 。
【分析】(1)铜灼烧生成氧化铜;
(2)根据化学反应的原理以及反应的特点来分析;
(3)根据酸的性质来分析。
【解答】解:(1)铜灼烧生成氧化铜,“灼烧”的主要目的是将铜转化为氧化铜,故答案为:将Cu转化为CuO;
(2)“酸溶”的原理是氧化铜能与稀硫酸反应生成硫酸铜和水,化学方程式为CuO H2SO4=CuSO4 H2O,该反应是由两种化合物相互交换成分生成两种新物质的化合物,因此属于复分解反应;故答案为:CuO H2SO4=CuSO4 H2O;复分解反应;
(3)过滤后的滤液中含有硫酸铜和硫酸,加入过量的铁屑时,铁与硫酸铜反应生成铜和硫酸亚铁,铁与硫酸反应生成硫酸亚铁和氢气,因此“转化”生成气体X的成分为氢气;故答案为:氢气(或H2)。
【点评】本题难度不是很大,理解回收含铜废料中的铜的部分实验流程图,熟练掌握酸的化学性质、金属的化学性质等是正确解答本题的关键。
13.(10分)其兴趣小组同学在老师的指导下,进入实验室对碳酸钙进行了一系列探究。回答下列问题:
Ⅰ.碳酸钙与盐酸反应
(1)装置A中仪器a的名称为 锥形瓶 。
(2)装置B中的现象是 石蕊试液变红 。
(3)装置C若用于检验生成的气体,其中试剂为 澄清石灰水 (写名称),发生反应的化学方程式为 CO2 Ca(OH)2=CaCO3↓ H2O 。
Ⅱ.碳酸钙分解
碳酸钙在电炉中高温煅烧一段时间后,对剩余固体进行探究。
【提出问题】剩余固体成分是什么?
【猜想与假设】猜想一:全部是碳酸钙
猜想二:是碳酸钙和氧化钙的混合物
猜想三:全部是氧化钙
【设计并完成实验】
实验操作 | 实验现象 | 解释与结论 |
步骤一:取剩余固体于试管中,加水振荡后静置 | 底部有白色不溶物 | \ |
步骤二:取上层清液于另一试管中,滴加氯化铜溶液 | 有 蓝色沉淀产生 | 上层清液中一定含有氢氧化钙 |
步骤三:取部分底部白色不溶物于第三支试管中,滴加过量稀盐酸 | 有气泡产生 | 白色不溶物中一定含有 碳酸钙 |
【实验结论】正确的猜想是 猜想二 。
【交流与反思】小芳同学认为,步骤二中还可滴加其他试剂用来替代氯化铜溶液,该试剂可以是 无色酚酞溶液 (写一种即可);小华同学认为,只需完成步骤一和步骤三即可获得相同实验结论,他的依据是 氧化钙和水反应放热,温度升高,即可知道剩余固体中有氧化钙 。
【拓展与分析】查阅资料:生石灰质量的优劣常采用“活性度”来衡量。“活性度”的测定方法:取一定质量的生石灰,加入一定量的水,用一定溶质质量分数的盐酸中和,记录所消耗盐酸的体积(单位为mL)。消耗盐酸的体积数越大,“活性度”越高。
测得煅烧产物(CaO)的活性度,数据见如表。
煅烧温度 活性度 煅烧时间 | 1050℃ | 1100℃ | 1150℃ | 1200℃ | 1250℃ | 1300℃ |
12 min | 790 | 836 | 868 | 808 | 454 | 412 |
16 min | 793 | 856 | 871 | 845 | 556 | 530 |
20 min | 795 | 863 | 873 | 864 | 617 | 623 |
石灰石煅烧的最佳温度范围一般为1100℃~1200℃的证据是 燃烧时间长短不同,在1100℃~1200℃范围内生石灰的活性度均高 。