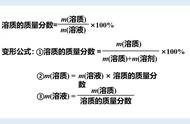
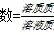蒸馏,用于分离沸点不同而又相溶的液态混合物,也可分离固液混合物。例如分离乙醇和水,利用蒸馏水制备纯净水。蒸馏时需要注意1、温度计水银球上沿与支管口下沿平齐;2、加沸石;3、冷凝水“下进上出”。

萃取、分液,萃取是利用溶解度差异把溶质从一种溶液提取到另一种溶液中,分液用于分离互不相溶的两液体。例如用CCl4萃取碘水溶液中的碘,需要注意1、萃取剂对溶质的溶解能力要大于原溶剂;2、萃取剂与原溶液不互溶;3、萃取剂与溶质、原溶液不发生反应。

(2)提纯化合物的基本要求
“过量”,为了除尽杂质,除杂试剂要添加过量。
“后除前”,后面加入的试剂能够把前面加入的试剂一并除去。
沉淀完全的判断方法,在上清液中滴加沉淀剂不再有沉淀生成时为沉淀完全。

典型例题,判断对错,请各位同学先暂停视频,自己先尝试判断。
好了,我们一起来看,第一题,利用装置1除去Cl2中混合的少量HCl。很明显,NaOH不仅会与混合的HCl发成反应,还会与氯气发生反应。因此,第一题错误。
第二题,利用装置2蒸干氯化铵溶液来制备氯化铵晶体,我们知道氯化铵受热易分解为氨气和氯化氢,因此用装置2不能得到氯化铵晶体。所以第二题也是错误的。
再来看第三题,利用装置3制备纯净的CO2气体。乍一看之下似乎没有问题,但是通过仔细读题我们会发现题中要求的是制备纯净的二氧化碳气体,而装置3中制备的二氧化碳气体中会不可避免的混有少量的氯化氢气体和水蒸气,并不符合题目要求。而若制备纯净的CO2则还需要将制备出的气体通过纯化装置才能达到要求。因此这道题也是错误的。
我们来看最后一题,利用装置4分离CCl4萃取碘水后的有机层和水层。装置4是一套完整的分液装置。因此这道题是正确的。