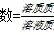1. 有关物质的量(mol)的计算公式
⑴ 物质的量(n)质量(m)摩尔质量(M)和物质所含微粒数(N)之间的换算关系
物质的量(mol)=物质的质量(g)÷物质的摩尔质量(g/mol)
或M=m÷n
n=m÷M
或 m=n×M
⑵ 物质的量(n)、阿伏加德罗常数(NA)、微粒数(N)之间有换算关系
物质的量(mol)=微粒数(个)÷6.02×10∧23(个/mol)
n=N÷NA
或 N=n×NA
或 NA=N÷n
⑶ 在标准状况下,气体的物质的量(n)、气体体积(V)、气体摩尔体积(Vm)的换算关系
气体物质的量(mol)=标准状况下气体的体积(L)÷22.4(L/mol)
n=V÷22.4
或V=n×22.4
⑷ 物质的量浓度C(B),溶质的物质的量n(B),与溶液体积(V)的换算关系:
溶质的物质的量(mol)=物质的量浓度(mol/L)×溶液体积(L)
n(B)=C(B)×V
或C(B)=n(B)÷V
或V=n(B)÷C(B)
⒉ 标准状况下气体的密度
ρ(g/L)=气体的摩尔质量(g/mol)÷气体摩尔体积(L/mol)=M/22.4mmol/L
ρ(g/L)=M÷22.4mmol/L
标准状况下气体的摩尔质量
M=22.4ρmol/L

⒊ 平均摩尔质量或平均式量的计算公式
⑴ 已知混合物的总质量m(混)和总物质的量n(混):
M=m(混)÷n(混)
说明:这种求混合物平均摩尔质量的方法,不仅适用于气体,而且对固体或液体也同样适用。
⑵ 已知标准状况下,混合气体的密度ρ(混):
M=22.4×ρ(混)
注意:该方法只适用于处于标准状况下(0℃,1.01×105Pa)的混合气体。
⑶ 已知同温、同压下,混合气体的密度与另一气体A的密度之比D(通常称作相对密度):
D=ρ(混)÷ρ(A)=m(A)÷n(A)
则M=D×M(A)
⑷ 阿伏加德罗定律及阿伏加德罗定律的三个重要推论。
①恒温、恒容时:
P1/P2=n1/n2
即任何时刻反应混合气体的总压强与其总物质的量成正比。
②恒温、恒压时:
V1/V2=n1/n2
即任何时刻反应混合气体的总体积与其总物质的量成正比。
③恒温、恒容时:
ρ1/ρ2=Mr1/Mr2
即任何时刻反应混合气体的密度与其反应混合气体的平均相对分子质量成正比。
⑸ 混合气体的密度ρ混=混合气体的总质量m(总)÷容器的体积V
(6) 混合气体的平均相对分子质量Mr的计算。
⑴ Mr=MA×a% MB×b% …
其中MA、MB分别是气体A、B的相对分子质量,a%、b%分别是气体A、B的体积(或摩尔)分数。
② Mr=混合气体的总质量(g)÷混合气体总物质的量(mol)

⒋ 有关溶液的计算公式
⑴ 基本公式
①溶液密度(g/mL)=溶液质量(g)÷溶液体积(mL)
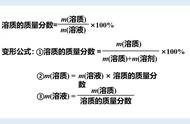
②溶质的质量分数=溶质质量(g)÷(溶质质量+溶剂质量)(g)×100%
③物质的量浓度(mol/L)=溶质物质的量(mol)÷溶液体积(L)
C(B)=n(B)÷V
或 n(B)=C(B)×V
或V=n(B)÷C(B)
⑵ 溶质的质量分数、溶质的物质的量浓度及溶液密度之间的关系:
某一溶液中溶质的质量分数ω(B)、溶质的物质的量n(B)和溶液密度(ρ)的换算关系
①溶质的质量分数=物质的量浓度(mol/L)×1(L)×溶质的摩尔质量(g/mol)÷1000(mL)×溶液密度(g/mL)×100%
②物质的量浓度=1000(mL)×溶液密度(g/mL)×溶质的质量分数÷溶质摩尔质量(g/mol)×1(L)
n(B)=1000×ρ×w(B)÷M
或W(B)=n(B)×M/1000ρ×100%
或ρ=n(B)×M/1000×w(B)
⑶ 溶液的稀释与浓缩的计算(各种物理量的单位必须一致):
原理:稀释或浓缩前后溶质的物质的量不变。
①浓溶液的质量×浓溶液溶质的质量分数=稀溶液的质量×稀溶液溶质的质量分数(即溶质的质量不变)
②浓溶液的体积×浓溶液物质的量浓度=稀溶液的体积×稀溶液物质的量浓度
C(浓)×V(浓)=C(稀)×V(稀)
注意:V浓、V稀的单位可以是L或 mL,但必须左右一致。
⑷ 任何一种电解质溶液中:阳离子所带的正电荷总数=阴离子所带的负电荷总数(即整个溶液呈电中性)