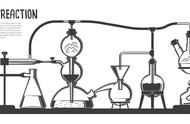
第13题图
(1) 请改正图中的错误① 、② 。
(2) 操作步骤:
A:计算:所称取氯化钠的质量,水的体积。
B:称量:用托盘天平称量氯化钠。
C:溶解:用量筒来量取所需的水(水的密度为1 g/cm3),量筒的规格是 (选填“10 mL”“50 mL”或“100 mL”);量水时,量筒必须平放,视线要与液体 保持水平;溶解氯化钠要用到玻璃棒,其作用是__________。
D:装瓶贴签。
【重点设问补充】
(3)如果配制的盐水中,NaCl的质量分数小于5%,则可能造成该误差的原因有 (至少写出一条)。
(4)此题的所配溶液,也可用10%的氯化钠溶液 克,然后加水稀释得到。
14. (2019贵州三州联考改编)实验室利用下图所示装置进行相关实验。

第14题图
回答下列问题:
(1)写出装置图中标号仪器名称:① 。
(2)用高锰酸钾制氧气,应选用的发生装置是 (填字母序号),该反应的化学方程式为 。
(3)常温下,用锌和稀硫酸反应制取氢气,若要随时控制反应的发生和停止,应选用的发生装置是 (填字母序号,下同),点燃氢气前必须验纯,为确保安全,最好选用装置 所示方法收集氢气。
【重点设问补充】
(4)上述装置既能用来制取氧气,又能用来制取二氧化碳的发生装置是 。
(5)B装置中的长颈漏斗伸入液面以下的目的是 。
(6)可用E装置收集的气体的特点是__________________。
15. 某研究学习小组对“NaOH溶液与稀H2SO4溶液是否恰好反应”进行实验探究。

第15题图
(1)如图是稀硫酸与氢氧化钠反应的实验过程。
①图中仪器A的名称是 。
②向A中加入10 mL NaOH溶液,并滴入3滴酚酞溶液,再向其中慢慢滴入稀硫酸,并用玻璃棒不断搅拌,使溶液混合均匀,直至溶液的颜色由红色恰好变成 色为止,表明两者发生了反应,该反应的化学方程式为____________________。
(2)为探究上述酸碱反应后,硫酸是否过量。设计了如下两种方法:
方法①:取少量反应的溶液,用pH试纸检验,测得pH<7,表明硫酸过量。
方法②:取少量反应的溶液,向其中滴加适量的BaCl2溶液,可观察到有白色沉淀产生,表明硫酸过量。上述两种方法中,你认为正确的是方法 (选填“①”或“②”)。请说明另一种方法不合理的原因__________________。
【重点设问补充】
(3)设问(2)中除了方法①②外,还可选用 来探究上述酸碱反应后,硫酸是否过量。
(4)若在上述实验中将稀硫酸滴入氢氧化钠溶液中,观察到有少量气泡产生,则可能的原因是 。
参考答案
1. (1)小 (2)搅拌,使热量尽快散失 液滴飞溅 (3)2H2O2 MnO2 2H2O+O2↑ 可以控制反应速率 (4)木条复燃 二氧化碳(或氢气)
2. (1)集气瓶 黑 (2)2H2O通电 2H2↑+O2↑ 负 (3)②③① (4)细沙 (5)装置漏气使装置外的空气进入瓶内(或红磷量不足等合理即可) 不能,氧气不足时,碳与氧气反应生成一氧化碳,不能被氢氧化钠溶液吸收(合理即可)
3. (1)烧杯②中溶液变红 氨气分子不断运动,进入滴有酚酞的蒸馏水中形成碱性的氨水,使溶液变红 (2)吸收生成的SO2,防止污染空气 (3)红色粉末变为黑色 CO2+Ca(OH)2 === CaCO3↓+H2O (4)防止澄清石灰水倒吸入热的玻璃管内,使玻璃管炸裂
4. (1)密度比空气大 不燃烧也不支持燃烧 (2)滤纸破损(或漏斗内液面高于滤纸边缘等合理即可) (3)不一定 (4)氢氧化钠溶液已变质
5. (1)氧化钙与水反应放出大量的热使气球膨胀 CaO+H2O === Ca(OH)2 (2)防止收集的气体中混有空气 (3)有固体析出 不饱和 (4)导管口一有气泡冒出就开始收集(合理即可) (5)有固体析出(或溶液变浑浊)
6. (1)水、氧气 (2)下降 平衡 CO2+NaOH === Na2CO3+H2O (3)氧化钙(合理即可)
7. (1)铝片 大于 (2)化学 (3)多 木条燃烧更旺 (4)氧气在水中的溶解度比氢气大(或有少量氧气溶解在水中等合理即可) 化学 导电性
8. (1)铁架台 2KClO3 =====MnO2△ 2KCl+3O2↑ (2)温度达到可燃物的着火点 (3)弱 Cu、AgNO3 (4)燃烧需要可燃物
9. (1)起密封作用,调节锥形瓶内气压,防止瓶内压强过大,使瓶塞迸出 (2)两支试管中溶液均变红 碳酸钠溶液显碱性(合理即可) (3)作对照 不能,酚酞溶液在中性或酸性溶液中不变色 (4)红磷燃烧放出热量,导致气球变大,气球所受浮力增大,天平右倾
10. (1)ABDC (2)搅拌,加快溶解 (3)转移时有溶液洒出(合理即可) (4)易溶于水 (5)小于
11. (1)木炭在氧气中燃烧生成二氧化碳 二氧化碳能与石灰水发生化学反应(或二氧化碳能使澄清石灰水变浑浊)(合理即可) (2)空气和二氧化氮气体中的分子在不断运动 (3)加入两种溶剂的量(或质量、体积)相等 B
12. (1)搅拌,使液体受热均匀,防止因局部温度过高造成液滴飞溅 (2)2H2+O2 点燃 2H2O 检验纯度 (3)铜生锈需要有氧气参与 (4)二氧化碳能溶于水且与水反应,使压强减小,塑料瓶也会变瘪 (5)水 小
13. (1)瓶盖倒放 左盘放药品、右盘放砝码 (2)50 mL 凹液面的最低处 搅拌,加速溶解 (3)氯化钠未称量够(或量取水时仰视读数或转移氯化钠固体时有撒出等合理即可) (4)25
14. (1)长颈漏斗 (2)A 2KMnO4 △ K2MnO4+MnO2+O2↑ (3)C D (4)B (5)防止生成的气体从长颈漏斗溢出 (6)密度比空气小
15. (1)①烧杯 ②无 2NaOH+H2SO4 === Na2SO4+2H2O (2)① 反应生成的硫酸钠也能和氯化钡溶液反应生成白色沉淀,无法确定是稀硫酸参与反应 (3)活泼金属(或碳酸盐或碳酸氢盐) (4)氢氧化钠已变质,生成的碳酸钠与稀硫酸反应生成二氧化碳气体
来源网络,版权归原作者所有。