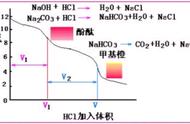
滴定分析法是将一种已知准确浓度的试剂溶液,滴加到被测物质的溶液中,直到所加的试剂与被测物质按化学计量定量反应为止,根据试剂溶液的浓度和消耗的体积,计算被测物质的含量。
滴定前,先配点药水。

1,配制EDTA滴定液
①可加热促使溶解,先浓配后稀释,摇匀后放24h为好,使其充分稳定。
②标定前氧化锌炽灼一定要到800℃,色泽应达鲜黄绿色,否则其中二氧化碳难以除尽。
③注意pH值变化,先滴加氨试液中和盐酸后加水稀释。
④铬黑T粉末放置不能过久,否则灵敏度差,指示液应逐滴加,充分振摇。
2,配制醇制氢氧化钾滴定液
①因AR级KOH标示含量为82实际上均为80左右,所以应为理论量355g。
②乙醇中醛类受光线作用呈深浅不同黄色故乙醇需精制无醛乙醇,精制后应立即放冷配制,制法见中国药典2000年版附录。
③防止二氧化碳与乙醇挥发,光照影响,应贮存于橡皮塞棕色玻璃瓶中,而且临用新标定。
3,配制四苯硼钠滴定液
①加新制Al(OH)3凝胶,使滤液澄清,强力振摇使溶解完全,先滤上清液。
②做好空白,滴定中特别是近终点速度要很慢,注意观察色泽变化,贮存期间出现浑浊应重新标定。
4,配制亚硝酸钠滴定液
①加无水碳酸钠作稳定剂用,使pH值保持在10左右,铂电极应临用前活化好。
②在试样加入前加KBr以促进反应。
③室温应30℃用胶管连接滴定管插入到液面下2/3处避免硝酸分解,计算好理论量“先快后慢”特别是近终点,逐滴加入,并搅拌。
5,配制草酸滴定液
①酸化应用硫酸,不可用硝酸或盐酸(硝酸有氧化性而盐酸易被高锰酸钾氧化)。
②近终点前加速反应加热可用水浴,直火加热温度难以控制,且温度太高草酸分解而使结果不准确。
6,配制氢氧化钠滴定液
①用饱和氢氧化钠液制备应新沸冷水制成而且应陈化6小时左右。排除碳酸钠干扰与二氧化碳。
②制备饱和氢氧化钠时应分多次加入氢氧化钠固体,过饱和后应放置三天后取上清液,应一次取出避免倒流而冲浑液体。
③也可用新制热蒸馏水,但制好后应放至室温,尽量避免二氧化碳干扰。
④基准应在玛瑙乳钵中研细,利于溶解,在终点前基准应全溶解,否则结果有误。
⑤标定前贮存聚乙烯塑料瓶中,用虹吸法取用,进气管前端用钠石灰和棉花过滤,定期或钠石灰变色后更换,防止二氧化碳影响浓度。
7,配制重铬酸钾滴定液
①基准应先研细,在120℃干燥至恒重,放冷后立即称量配制。
②最好是棕色瓶,浓配摇匀使溶后再加水至刻度。
8,配制烃铵盐滴定液
①氮化二甲基苄基烃在溶解过程应逐步缓加,防止粉末漂浮,应加强搅拌,必要时放入超声波助溶,先浓配后稀释为好。
②标定时氯化钾用基准或色谱纯,其结果即准确且终点明确。

9,配制高氯酸滴定液
①是碱性基因的有机化合物。加入醋酐量应为理论量12~13倍,一般市售高氯酸含量普遍偏低,1000mL配制理论量85ml,实际工作中取用96-98ml,导致含水增大,所以应加入12倍左右的实际用量而保证含水量合格。
②配制中先加醋酸将高氯酸稀释,以免反应剧烈,色泽变黄导致分解,滴加醋酐先振摇后滴加,速度宜慢不宜快。
③避光保存或用黑布套在棕色瓶中,若溶液变成浅黄色,即,为分解不能再用。
10,配制高锰酸钾滴定液
①煮沸过程要保持一段时间,促使其中还原性杂质反应完全。以免在以后贮存中引起浓度改变。过滤目的除去二氧化锰。
②加新沸水目的除水中氧,以免标定过程中草酸钠被氧化使浓度偏高。
③酸度调节用硫酸为好,总的浓度控制在0.5mol/L,酸度低反应太慢,酸度太高又容易使高锰酸分解。
11,配制硝酸银滴定液
①宜避光配制,注意保护不要使皮肤或衣服上被污染,因为除掉较难。
②标定系吸附指示剂,所以应保护生成氯化银呈胶体状肪,应在氯化钠溶解后再加糊精。
③宜在中性或弱碱性中进行,加碳酸钙以利于形成荧光黄阴离子指示终点。
④滴定中也应避光,特别是强光照射。
12,配制硫代硫酸钠滴定液
①煮沸应保持5分钟左右,利于清除二氧化碳与氧气,加碳酸钙作为稳定剂,pH值应保持在弱碱性约pH值9~10防止分解。
②放置30天以上是促反应完全,过滤除杂质,滴定过程取用50mL滴管为好。
③标定中应避光,因碘化钾为强酸性,在静置过程也释放碘,应同时作空白,若贮存滴定液出现浑浊现象,即也分解不能用。
13,配制硫酸亚铁滴定液
①硫酸亚铁在空气中风化、氧化现象,配制应注意量的取用。
②本溶水溶液不稳定,但在酸性条件下稳定,所以加硫酸:水40:20混合液保持稳定。
14,配制硫酸铈铵滴定液
①配制先将溶液溶解完全后加硫酸防水解。
②因属于强氧化剂,用三氧化二砷标定,加氯化碘作催化剂,指示剂邻二氮菲中因含有少量铁也消耗滴定液使结果不准确,应注意加量,近终点加热是为了加速反应。
15,配制硫酸锌滴定液
硫酸锌应取无水硫酸锌,应注意区别无水或水硫酸锌,加盐酸是防止水解。
16,配制碘滴定液
①碘在水中不溶且有挥发性,配制用利用碘化钾的水溶液形成三碘络离子而溶解并降低挥发性,配制中先将碘化钾置锥形瓶中加水溶解成高浓度溶液,碘要在乳钵中研细后再加入锥形瓶中使溶解,振摇完全溶解后再加盐酸过滤
②加盐酸保持微酸性,防止碘酸盐,同时也中和标定中稳定剂碳酸钠。
③因有腐蚀性发性应贮存在棕色瓶中放置一周后标定,应避免有机物。
④三氧化二砷难溶于水,加氢氧化钠液加热使成亚砷酸钠而溶,加硫酸调节pH值是因为碘量法不宜在碱性溶液中进行''中和后加碳酸氢钠使其中性或微碱性pH8左右。
⑤配制淀粉指示剂加热时间宜短,应在冰浴快速冷却,这样灵敏高,终点易于观察。
17,配制溴滴定液
①取用在毒气柜或通风柜中进行,避免吸入中毒,避免手直接触及,避免伤害。
②若直接滴定可临用新标,若用间接法,可不标定,因为有已标定硫代硫酸钠。
这些注意事项你可能需要特别注意!
(1)分析实验所用的溶液应用纯水配制,容器应用纯水洗三次以上。
(2)溶液要用带塞的试剂瓶盛装。
(3)配制好的试剂应及时盛入试剂瓶,试剂瓶上必须有标液名称、浓度和配制人,配制日期,有效期限。
(4)溶液储存时应注意不要使溶液变质。
(5)配制硫酸、磷酸、硝酸、盐酸等溶液时,应把酸倒入水中。
(6)用有机溶剂配制溶液时(如,制指示剂溶液),可以在热水浴中温热溶解,不可直接加热。
(7)应熟悉一些常用溶液的配制方法及常用试剂的性质。
(8)不能用手直接接触腐蚀性及有剧毒的溶液,剧毒废液应作解毒处理,不可直接倒入下水道。

Question:
几乎每周一次分析化学实验,全是滴定。我最夸张的一次做过六次滴定才保证有三组数据相对极差符合标准。看别人做完实验都走了,我手都滴酸了还没搞定。我最主要的问题就是很容易滴过了。要耐心这种大方向的话我也每次都提醒自己。有没有什么小建议可以帮到我的?比如到底要不要看滴定管的刻度,滴定速度快和速度慢怎么来判断这些细一点的点?
Answer:
1.摇瓶子时,应微动腕关节,使溶液像一个方向做圆周运动,但是不要使瓶口接触滴定管,溶液也不得溅出来;
2.滴定时左右不能离开旋塞让液体自行流下;
3.注意观察液滴落点周围溶液颜色变化。开始时应边摇动边滴,滴定速度可稍快(每秒3-4滴为宜),但是不要形成水流。接近终点时应该为加一滴,摇几下,最后,每加半滴,即摇动锥形瓶,直至溶液出现明显颜色变化,准确到达终点为之。
4.滴定时不要去看上边滴定管的体积,而不顾滴定反应的进行,加半滴溶液的方法如下:微微转动活塞,使溶液悬挂在出口嘴上,形成半滴,有时还不到半滴,用锥形瓶内壁将其刮落。
5.每次滴定最好从0.00ml处开始,也可以固定使用滴定管某一段,以减小误差。