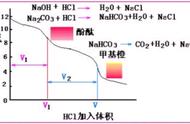
适合滴定分析的化学反应应该具备以下几个条件
(1)反应必须按方程式定量地完成,通常要求在99.9%以上,这是定量计算的基础。
(2)反应能够迅速地完成(有时可加热或用催化剂以加速反应)。
(3)共存物质不干扰主要反应,或用适当的方法消除其干扰。
(4)有比较简便的方法确定计量点(指示滴定终点)。

常见滴定分析法有哪几类?
1.酸碱滴定法
滴定分析法中,酸碱滴定最基本。
中心问题:“酸碱平衡”,本质是酸碱之间的质子传递。
2.配位滴定法
主要是:EDTA的结构、性质、配位平衡、稳定常数、滴定曲线、指示剂的选择及消除干扰的方法。
重点:配位平衡。在配位滴定中, 除主反应外, 还有各种副反应干扰主反应的进行, 反应条件对配位平衡有很大的影响。
3.氧化还原滴定法
氧化还原滴定法的核心仍然是平衡,是以电子转移为依据的平衡,反应条件对平衡的影响很大。
4.沉淀滴定法
沉淀滴定法的核心是沉淀平衡。
重点是银量法, 根据确定终点的方法不同, 可分为摩尔法、福尔哈德法、吸附指示剂法。
酸碱、配位、氧化还原、沉淀滴定之联系与区别
滴定分析的共同特点是在滴定过程中,被测离子浓度呈现出规律性变化。只要重点掌握酸碱滴定过程中pH值计算,其它几种滴定方法可依相同的思路加以解决。
通常把滴定过程分成四个阶段,即:
(1)滴定开始前;
(2)滴定开始至计量点前;
(3)计量点时;
(4)计量点后。
要了解滴定过程被测离子浓度的变化情况,首先必须弄清滴定各阶段溶液组成的变化情况,然后根据相应组成的计算公式计算。
特别应注意的是:
滴定过程中达到计量点时滴定剂由不足99.9%到过量0.1%之间pH(PM,PE)的变化范围,即滴定突跃,这是选择指示剂的重要依据。
酸碱指示剂变色范围?影响因素?
酸碱指示剂的颜色随溶液PH的改变而变化,其变色范围越窄越好,在化学计量点附近,PH稍有改变,指示剂立即由一种颜色变为另一种颜色,指示剂变色敏锐。
表:常用的酸碱指示剂及其变色范围~

影响指示剂变色范围的因素
1、温度:
温度改变,指示剂的变色范围也随之改变。
例如:
18℃时,甲基橙的变色范围为3.1-4.4,
100℃时,则为2.5-3.7。
2、溶剂:
指示剂在不同溶剂中变色范围不同
3、指示剂用量:
浓度小:颜色变化灵敏;
浓度大:终点颜色变化不敏锐;
指示剂用量少一点为佳。
滴定分析操作注意事项
一、仪器的检漏(滴定管、容量瓶)、洗涤
滴定管和容量瓶使用之前应当先检漏。
具体检漏方法想必你早就知道,只说说注意事项哈:
1、凡士林不应涂太多,否则会堵塞小孔;
2、旋动旋塞时应有一定的向旋塞小头部分方向挤的力,以免来回移动旋塞,使塞孔受堵;
3、滴定管、容量瓶、移液管(吸量管)、锥形瓶都需洗涤。