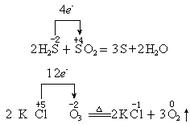
1、定义,凡是有化合价升降的化学反应都是氧化还原反应。
化合价升降的本质是电子的转移,所以也可以说成:凡是有电子转移的反应都是氧化还原反应。
这里要强调一下,是否有化合价升降,或者说是否有电子转移是判断一个反应是不是氧化还原反应的唯一途径,其它的判断方法统统不好使,就好像考大学只看你高考考了多少分,不会看你家有几套房,也不会看你爸是某刚还是某双江。
我们重点来看表示方法:(1)双线桥法:表示同一元素的原子间电子得失或偏移的方法。
以一氧化碳还原氧化铁为例,可以写出如图中所示的双线桥式。
在书写双线桥式的时候需要注意这几点:箭头必须由反应物指向生成物,且两端为同种元素。

在“桥”上标明电子的“得”“失”,且得失电子总数相同。

电子转移用“a×b e-”这样的形式表示,a代表发生氧化还原反应的原子的个数,b代表每个原子得到或失去电子的个数。(a或b=1时可省略不写)

箭头方向仅仅表示电子转移前后的变化,不代表电子转移方向。