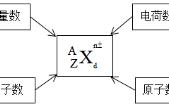
1.离子晶体一般是离子化合物
2.分子晶体一般是共价化合物
3.原子晶体有 硅 碳 二氧化硅❗️(有且仅有这三个)❗️
4.A和B的混合物中求某原子的数目用极值法
5.四氯化碳,四氧化二氮,二氧化氮,溴,三氧化硫,己烷,氟化氢,本,在标况下非气态
6.

7.注意区分同素异形体和同位素的区别
同素异形体顾名思义同种元素构成的不同单质例如氧气和臭氧
同位素是同种元素的不同原子。例如碳12和碳13
8.物质组成
①由同位素组成的不同原子构成的单质是纯净物,例如碳12和碳13组成的是纯净物
②冰水混合物,结晶水化物(如五水硫酸铜)属于纯净物
③高分子化合物属于混合物
煤的干馏蛋白质的变性属于化学变化
渗析,盐析,潮解是物理变化
9.胶体区别于其他分散系的本质特征是直径而不是丁达尔效应。
10.向沸水中逐滴加入三氯化铁饱和溶液,继续煮沸至溶液呈红褐色的氢氧化铁胶体。
11-13(只对于高中阶段来说)
11.有机酸是弱酸,沉淀碱(如碳酸钙)是弱碱
- 大部分金属氧化物是碱性氧化物
- 非金属氧化物是非电解质(例如二氧化硫)
- 与碱反应只生成盐和水的物质是酸性氧化物
- 浓硫酸具有强氧化性反应,一般生成二氧化硫
- 氯离子与氨水反应,无论氨水是否过量,都生成氢氧化铝
- 离子共存问题(请忽略我丑陋的字)

18.甲基层变红显酸性
19.常考四种离子的检验干扰措施
①检验硫酸根
先加入盐酸酸化排除银离子的干扰,再加入氯化钡,产生白色沉淀,则说明有硫酸根的存在❗️这里只能是加入氯化钡,不能加入其他的如碳酸钡亚,硫酸钡等
②检验溶液中含有的是亚硫酸根,而不是硫酸根的方法
取少量溶液加入氯化钡产生白色沉淀,再加入稀盐酸沉淀完全溶解并产生无色刺激性气体则可说明溶液中含有的是亚硫酸根,而不是硫酸根。
③碳酸根的检验
先加入氯化钙或氯化钡排除碳酸氢根的干扰,再加入盐酸产生无色无味气体,排除亚硫酸根的干扰,最后通入澄清石灰水
④二价铁离子的检验
溶液中含二价铁离子和三价铁离子,可加入酸性高锰酸钾溶液,若褪色,则说明溶液中含有的是二价铁离子
20.关于金属的常考方程式