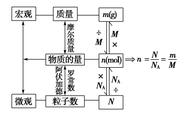
全部换成符号,得:

关卡四 如何理解“物质的量是连接微观与宏观的桥梁”?
要理解这句话,我们需要先掌握如下知识:1mol任何粒子的质量 = 这个粒子的原子量或分子量(克)(这个结论很重要,需要先记住后理解。至于为什么是这样,关卡五有解读)
比如1mol碳12原子的质量=12克,1mol氧原子的质量=16克,1mol氧分子的质量 =32克。
为什么说物质的量是连接微观与宏观的桥梁?
所谓在宏观和微观之间建立联系,是什么意思呢?
我们看一个例子:假设我们日常喝水的保温杯中有360g水(如一个360ml的保温杯装满4摄氏度的纯水就是360g),这里面有多少水分子呢?有20×6.02×10的23次方个水分子,或者说有20mol

水分子是微观的,一杯水,360g都是宏观的(g是我们日常生活中使用的单位,跟极小的微观粒子相比较,“克是宏观的。)。他们是通过20×6.02×10的23次方或者20mol联系起来的。20mol就是水分子的物质的量。
一图胜千言,请看下图:

图注:水分子是微观,单位“克”和一杯水是宏观
说明:关卡五的内容可以不用了解,高考也不会考。基础好,又有钻研精神的同学,建议阅读。目前基础不太牢固的同学,可以等将来基础更牢固之后,再来阅读。我们要永远只设置适当的“跳一跳”就能够得着的目标。
关卡五 为什么规定的是6.02×10的23次方这个数,而不是其他数?(不用了解)
这部分你需要先具备如下基础知识:关于原子量和分子量的知识,如,
H离子的原子量(即相对原子质量)是1
C12原子的原子量是12
O原子的原子量是16
氧分子的原子量是32
再强调一遍,这部分有些同学读的时候可能不能马上读懂,没关系,这部分不是那么重要。
为什么规定的是6.02×10的23次方这个数,而不是其他数?
简单的讲,是因为科学家发现1g质子(氢离子)中有6.02×10的23次方个质子(这里需要一个补充知识:一个质子的质量为1.672621637×10的24次方克,×6.02×10的23次方个 = 1克)。
于是科学家规定6.02×10的23方个为1mol。之所以规定6.02×10的23次方个为1mol,而不是规定其他的数,是因为这样规定有一个巨大的好处,那就是:规定6.02×10的23方个为1mol,那么1mol任何粒子的质量=这个粒子的原子量分子量(克)(比如1mol碳12原子的质量=12克,1mol氧原子的质量=16克,1mol氧分子的质量 =32克)
好的,整理一下思路。现在我们已知的是:①科学家发现1g质子(氢离子)中有6.02×10的23次方个质子 ②科学家规定6.02×10的23方个为1mol 。显然1mol质子的质量就是1g。
我们需要根据这些已知信息推出如下结论:1mol任何粒子的质量=这个粒子的原子量分子量(克)
为什么呢?我们以1mol碳12原子为例。
我们现在的已知条件是:①1mol质子的质量=1g ②1mol = 6.02×10的23方个。
我们需要推出的结论是:1mol碳12原子的质量 = 12g(12即为C12原子的原子量)
好的,我们现在已知1mol质子有1g,那么1mol碳12原子有几克呢?我们可以这样理解:因为1个碳原子里面有12个质子中子,所以1个碳原子的质量相当于12个质子的质量(质子和中子的质量看作相等。12即相对原子量),所以1mol碳12原子的质量是1mol质子质量的12倍。又因为1mol质子的质量是1g,所以1mol碳12原子的质量是12g
一图胜千言: