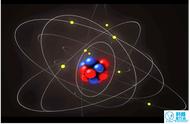
1897年英国物理学家汤姆森发现原子中存在电子,证明原子可分,并提出了“葡萄干布丁”的原子模型,认为原子是一个圆球状内充斥着正电荷,而带负电的电子像一粒粒葡萄干一样均匀相欠在其中。他对原子结构认识有以下几点:
①原子可以分为带负电的电子和带正电荷的物质;
②原子是个平均分布正电荷的球体,带负电的电子相嵌在其中;
③电子是静止不动的。
1.3、卢瑟福(1911年提出:核式模型或行星模型)

1909年著名物理学家卢瑟福通过α粒子散射实验(也叫金箔实验),提出了原子的核式模型。

α粒子散射实验:用一束带正电的α粒子去轰击金箔,发现大多数α粒子都能穿过金箔,且发生很小的偏转,很少的α粒子发生大的偏角,极少数α粒子发生超过90度的偏转,极个别的α粒子发生180度角偏转而反弹回来。
核式原子的结构模型的基本观点:
①原子质量几乎全部集中在直径很小的带正电的原子核上;
②原子内部大部分体积是空的;
③带负电的电子随意的绕带正电荷的原子核运动;
1.3、波尔原子模型(1913年提出:波尔量子化模型)

1913年波尔原子模型指出:电子不是随意占据在原子核的周围,而是在固定层面上运动。
波尔原子结构模型的基本观点:
①原子中的电子在具有确定半径的圆周轨道上,绕原子核运动;
②在不同轨道上的运动的电子具有不同的能量;
③当电子从一个轨道跃迁到另个轨道时,才会辐射或吸收能量。
1.4、现代电子云模型(1926年提出)