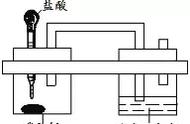
某同学将10g碳酸钙和氯化钙的混合物进行了如图实验,下列物质恰好完全反应,请计算:

(1)生成CO2气体的质量______g;
(2)反应后所得溶液中溶质质量分数为_____。

别偷懒哦
做完了才能看答案!

【答案】 2.2g 5%
【解析】(1)该实验中只有碳酸钙与稀盐酸发生反应生成二氧化碳和水,根据质量守恒定律,生成二氧化碳的质量为150g 53.2g 10g-211g=2.2g
(2)设10g样品中碳酸钙的质量为x,生成氯化钙的质量为y
CaCO3 2HCl == CaCl2 H2O CO2↑
100 111 44
x y 2.2g