一、选择题
1.家庭日常生活中经常用到的下列物质中,属于纯净物的是( )
A.调味用的食醋 B.餐饮用的啤酒
C.降温用的冰水共存物 D.炒菜用的铝合金锅
2.下列各组物质按单质、氧化物、混合物的顺序排列的是( )
A.金刚石、冰水混合物、石油 B.氮气、氧气、纯碱
C.稀有气体、二氧化碳、牛奶 D.钢、氧化镁、空气
3.下面所述的各物质中属于纯净物的是
A.纯净的空气 B."农夫山泉"矿泉水
C.用KMnO4制取O2后剩余的固体 D.冰水混合体
4.下列物质中,属于纯净物的是

5.下列物质属于混合物的是
A.矿泉水 B.冰水 C.高锰酸钾 D.氢氧化钙
6.液氧转化为氧气的过程中,发生的变化是
A.混合物变为纯净物 B.分子间的空隙增大
C.分子种类发生变化 D.分子总数增加
7.下列说法正确的是( )
A.工业上常采用分离液态空气法制氧气,该原理是利用氮气和氧气的密度不同进行分离
B.实验是制取气体的原料必须是纯净物
C.氧气的化学性质比较活泼,属于可燃物
D.空气质量报告中所列的空气质量级别越小,空气质量越好
8.下列有关仪器使用或用途的叙述中正确的是( )
A.试管:加热时所盛液体体积不超过试管容积的2/3
B.烧杯:给烧杯中的液体加热时需放置在石棉网上
C.酒精灯:熄灭酒精灯时可用嘴吹灭
D.滴瓶:为防止试剂污染,滴瓶的滴管在使用后要立即用水洗净
9.分子和原子的主要区别是( )
A、分子大、原子小 B、分子不停运动原子不运动
C、在化学反应中,分子可分,原子不可分 D、分子间有间隔,原子间没有
10.水由液态变成气态,由于( )
A、分子的大小改变 B、分子的质量改变
C、分子不断运动 D、分子间隔发生改变
11."金秋十月,丹桂飘香"。"飘香"这现象可说明( )
A、分子很小 B、分子间有间隙 C、分子是运动的 D、分子可再分
12.下列物质属于氧化物()
A、二氧化碳 B、三氧化二铁 C、金刚石 D、高锰酸钾
13.下列物质中属于纯净物的是
A.矿泉水 B.冰水 C.可乐饮料 D.澄清石灰水
14.用分子的知识解释下列现象,正确的是
A.降温能使水结成冰,是因为在低温下水分子静止不动
B.铁丝在空气中不燃烧而在氧气中却能燃烧,说明空气中和氧气中的氧分子化学性质不同
C.变瘪的乒乓球放入热水中能鼓起来,是由于分子受热体积变大
D.缉毒犬能根据气味发现毒品,是由于分子不断运动
15.下列各组物质中,前者是混合物,后者是纯净物的是
A.盐水 白酒 B.可乐汽水 二氧化碳
C.冰水混合物 液氧 D. 氮气 氧气
二、填空题
16.(4分)现有八种物质:①液态氧,②蒸馏水,③四氧化三铁,④过氧化氢溶液,⑤高锰酸钾加热制氧气后试管内的剩余物,⑥氮气,⑦氯酸钾,⑧清新的空气。用序号按下列要求填空:
(1)属于混合物的是 ;(2)属于纯净物的是 ;
(3)含有氧气的是 ; (4)空气中含量最多的物质是 。
17.物质是由微观粒子构成的,用分子、原子等相关知识回答下列问题
(1)分子和原子的主要区别是:在化学反应中 发生变化, 不发生变化,只能重新组合成新的 。
(2)从微观上解释混合物和纯净物。对于由分子构成的物质,混合物是由_______(填"同种分子"或"不同种分子"下同)构成的,纯净物是由 构成的。
18.(4分)有下列物质,①冰水混合物 ②一种黑色粉末 ③高锰酸钾完全分解后的固体剩余物 ④液氮 ⑤洁净的空气 ⑥铁水 ⑦五氧化二磷 ⑧呼出气体 ⑨澄清石灰水 ⑩稀有气体。用序号填空:属于纯净物的有 ;属于混合物的有 。
19. 将下列物质按要求分类(填序号)
①空气 ②液态氧 ③蒸馏水 ④过氧化氢 ⑤四氧化三铁 ⑥澄清石灰水 ⑦氯化钠 ⑧高锰酸钾完全分解后的固体残余物其中,属于混合物的是___________________;属于化合物的是____________________;属于单质的是_____________________;属于氧化物的是_______________________。
20.现有①液氧 ②液态空气 ③冰水共存物 ④二氧化锰 ⑤石灰水 ⑥氯酸钾 ⑦过氧化氢溶液 ⑧水银 (填错、填少、填多都不能得分)
其中属于混合物的有(填序号)___________,属于纯净物的有(填序号) ________________,
21.在下列空格里,用"原子、分子或离子"填空
(1)水是由_________构成的;氧气是由_________构成的;铁是由构成的
(2)带电的原子叫_________。
(3)保持二氧化碳化学性质的最小粒子是二氧化碳_________。
(4)化学变化中的最小粒子是_________。
三、简答题
22.(16分)(1)根据钠元素在元素周期表中的信息,将下图方框内①-⑤项内容补充完整:

(2)硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:

①t1℃时,两物质中溶解度较大的是 。
②t2℃时,两物质的等质量饱和溶液降温至t1℃,析出固体质量较大的是 的溶液。
③t2℃时,将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的 (填"饱和"或"不饱和")溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数 (填"变大"、"不变"或"变小")。
④欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是 。
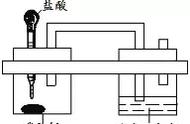
(3)某同学进行下图所示实验,证明酸碱发生反应的现象为:试管中溶液由 色变为无色,该反应的化学方程式为 。实验后测得试管中溶液的pH=2,该溶液中的溶质有 (写名称)。

四、推断题
23.(6分)下图中的物质均为初中化学常见的物质.其中甲、乙、丙、丁、戊均为单质,丙是空气中含量最多的气体。常温下,丁为黑色固体,戊为紫红色金属;G是一种具有刺激性气味的气体,其水溶液呈碱性,工业上用甲和丙化合制备G;农业上常用F改良酸性土壤(如图中部分反应条件已省略)。回答下列问题:

(1)D为 ;G为 。
(2)工业上用甲和丙化合制备G,反应中甲与丙的分子个数比为 ,在电解A实验中,
极产生物质乙。
(3)H和E反应生成C和戊的化学方程式
为 。
(4)工业上可以用甲和四氯化硅在高温条件下发生
置换反应来制取硅单质.此反应的化学方程式为
24.(5分)有一包白色粉末,可能是FeCl3、CaCO3、BaCl2、Na2SO4、KOH、KNO3中的一种或几种,为证明其组成,进行如下实验:

根据上述实验现象判断:
①白色固体中一定不含 ,一定含有 ,
可能含有 ;
②上述过程中通入CO2产生白色沉淀的化学式是 ;
③写出滴加稀盐酸白色沉淀全部溶解的化学方程式 。
参考答案
1.C
【解析】
试题分析:纯净物:由一种物质组成的,混合物:两种或多种物质组成的,C、降温用的冰水共存物是同种物质的不同状态,属于纯净物,故选C
考点:纯净物和混合物
2.A
【解析】
试题分析:混合物:由两种或两种以上的物质组成;单质:由同种元素组成的纯净物;氧化物:由两种元素组成,其中一种元素是氧元素的化合物。A、金刚石是单质碳,冰水混合物只是同种物质的两种不同状态,是氧化物,石油中含有多种物质,是混合物,故选A
考点:物质的分类
3.D
【解析】
试题分析:纯净物是一种物质组成的,混合物是两种或两种以上物质组成的物质,A选项纯净的空气 是由多种物质组成的; B."农夫山泉"矿泉水是由多种物质组成的; C.用KMnO4制取O2后剩余的固体室友锰酸钾和二氧化锰组成的; D.冰水混合体是一种物质组成的;故选择D
考点:纯净物和混合物的判定
4.D
【解析】
试题分析:混合物是由两种或两种以上物质组成的,纯净物是由一种物质组成的二者的本质区别时是否有一种物质组成,A加碘食盐由多种物质组成;B调和植物油是有多种物质组成的;C选项洗涤剂是有多种物质组成的;D选项干冰是由一种物质组成的,属于纯净物,故选择D
考点:纯净物和混合物的判定
5.A
【解析】
试题分析:A、矿泉水含有多种矿物质、含有多种可溶性物质,为混合物,符合题意; B、冰水混合物是由一种物质组成属于纯净物,不符合题意; C、高锰酸钾是由一种物质组成属于纯净物,不符合题意; D、氢氧化钙是由一种物质组成属于纯净物,不符合题意.故选:A.
考点:纯净物和混合物的判定
6.B
【解析】
试题分析:A、液氧与氧气都是由氧分子构成的,液氧与氧气属于同种物质都是纯净物,所以A不符合题意,故A错误; B、液氧转化为氧气,分子本身没变,分子之间的间距变大,所以B符合题意,故B正确; C、液氧转化为氧气,分子本身没变,没有新物质生成,所以显然化学性质不变,所以C不符合题意,故C错误; D、液氧转化为氧气,分子本身没变,分子的总数不会增加,只是分子之间的间距变大.所以D不符合题意,故D错误.故选:B.
考点:利用分子、原子的观点解决实际问题
7.D
【解析】
试题分析:A、工业上常采用分离液态空气法制氧气,该原理是利用氮气和氧气的沸点不同进行分离,错误; B、实验是制取气体的原料不一定纯净物,例如制取氧气使用过氧化氢溶液和二氧化锰的混合物,错误; C、氧气的化学性质比较活泼,不具有可燃性,不属于可燃物,错误; D、空气质量报告中所列的空气质量级别越小,空气质量越好,正确;故选D.
考点:氧气的工业制法、氧气的化学性质、空气污染及其危害
8.B
【解析】
试题分析:A、给试管内液体加热时,试管内液体量不能超过试管容积的1/3,故A错误; B、烧杯不能直接加热,给烧杯中的液体加热时需放置在石棉网上,故B正确; C、酒精灯的熄灭方法:用灯帽盖灭,不能用嘴吹灭,否则引起火灾,故C错误; D、滴瓶的滴管在使用后不能用水洗净,故D错误.故选B.
考点:常见仪器的名称及选用
9.C
【解析】本道题主要考察分子和原子的定义,区分分子和原子就看在化学变化中能否再分
10.D
【解析】分子大小和质量不会发生改变,之所以水存在三态变化是因为水分子间隔发生了变化;
11.C
【解析】分子的三个特点是:质量和体积都很小,总是在不断做运动,分子间有间隔,正因为分子在不停的运动,所以才能闻到花香;
12.A B
【解析】氧化物的定义是由两种元素组成,一种元素是氧元素,金刚石是单质,高锰酸钾由钾,锰,氧三种元素组成故金刚石和高锰酸钾不是氧化物;
13.B
【解析】
试题分析:由一种物质组成的物质属于纯净物,由多种物质组成的物质属于混合物二者的本质区别是是否由一种物质组成A、矿泉水里面除了水还有矿物质,故属于混合物; B、冰水混合物是水的不同状态的混合,但只有水一种物质构成,故属于纯净物; C、可乐饮料除了水,还含有二氧化碳等多种物质,故属于混合物; D、石灰水是氢氧化钙和水的混合,故属于混合物.故答案为:B.
考点:纯净物和混合物的判定
14.D
【解析】
试题分析:A、降温水结成冰是因为降温改变了分子间的间隔,而分子仍然是不断运动的,故A错误; B、铁丝在空气中不燃烧而在氧气中能燃烧,是因为空气中氧气浓度太小,无论是空气中的氧气还是纯氧气都是由氧分子构成的,同种物质的分子性质相同,故B错误; C、变瘪的乒乓球放入热水中能鼓起来,是由于分子受热之间的间隔变大,而分子体积不变,故C错误; D、缉毒犬能根据气味发现毒品,是由于分子不断运动,故D正确.故选D.
考点:分子的特征
15.B
【解析】
试题分析:A、盐水中含有氯化钠、水等物质,属于混合物;白酒中含有水、酒精等物质,属于混合物.故选项错误. B、可乐中含有水、蔗糖、碳酸等多种物质,属于混合物;二氧化碳中只含有一种物质,属于纯净物;故选项正确. C、冰水混合物(冰是固态的水)、液氧中均只含有一种物质,均属于纯净物.故选项错误. D、氮气、氧气中均只含有一种物质,均属于纯净物.故选项错误.故选:B.
考点: 纯净物和混合物的判定
16.(1) ④⑤⑧;(2) ①②③⑥⑦;(3) ①⑧;(4) ⑥
【解析】
试题分析:由一种物质组成的物质属于纯净物,由多种物质组成的物质属于混合物二者的本质区别是是否由一种物质组成,故(1)属于混合物的是④⑤⑧; (2)属于纯净物的是①②③⑥⑦; (3)含有氧气的是①⑧;(4)空气中含量最多的物质⑥。
考点:纯净物和混合物的判断、空气中气体的体积分数
17.(1)分子;原子;分子;(2)不同种分子;同种分子
【解析】
试题分析:(1)分子和原子的主要区别是:在化学反应中分子发生变化,原子不发生变化,只能重新组合成新的分子。(2)从微观上解释混合物和纯净物。对于由分子构成的物质,混合物是由不同种分子构成的,纯净物是由同种分子构成的。
考点:分子原子的区别、纯净物和混合物的区别
18.①④⑥⑦ ③⑤⑧⑨⑩
【解析】
试题分析:纯净物为一种物质组成的物质,混合物为有两种或两种以上物质组成的物质二者的本质区别是是否由一种物质组成;故属于纯净物的有①④⑥⑦;属于混合物的有③⑤⑧⑨⑩。
考点:纯净物和混合物的判定
19.①⑥⑧;③④⑤⑦;②;③④
【解析】
试题分析:混合物是有多种物质组成的物质,化合物是由多种元素组成的纯净物,单质时一种元素组成的纯净物;氧化物为两种元组组成其中一种是氧元素的化合物;在所提供的物质中属于混合物的是①⑥⑧;属于化合物的是③④⑤⑦;属于单质的是②;属于氧化物的是③④。
考点: 物质的分类
20.属于混合物的有(填序号)②⑤⑦,属于纯净物的有(填序号) ①③④⑥ ⑧。
【解析】
试题分析:混合物是由多种物质组成的物质,纯净物是一种物质组成的物质,二者的本质区别时是否有一种物质组成;其中属于混合物的有②⑤⑦;属于纯净物的有(填序号) ①③④⑥ ⑧。
考点:物质的多样性
21.(1)分子 分子 原子 (2)离子 (3)分子 (4)原子
【解析】本题考查了化学用语的使用和理解。要区分宏观概念和微观粒子,元素是宏观概念,它是组成物质的基本单位;分子、原子和粒子是构成物质的三种微观粒子。其中原子通过得失电子后变成离子,原子可以直接构成分子,原子是化学变化中的最小粒子。
22.(1)①22.99②11③1④失⑤Na (2)①氯化钾②硝酸钾③饱和 不变④温度不低于t1℃
(3)红 HCl NaOH==NaCl H2O 氯化钠、氯化氢和酚酞
【解析】
试题分析:(1)在元素周期表中的一格中,左上角的数值为其原子序数(质子数或核电荷数);右上角的符号为其元素符号;中间的汉字为该元素的元素名称,最下方的数值表示该元素的相对原子质量。所以①钠的相对原子质量为22.99;②在结构示意图中,圆圈内的数值X为该原子的质子数,可根据前面的图知道其质子数为11;③Y表示钠原子的最外层电子数。因为在原子中质子数=核外电子数;即11=2 8 Y;所以Y为1;④因为钠原子的最外层电子数为1,小于4个,所以易失1个电子。⑤钠离子是由钠原子失去最外层的1个电子形成的,带一个单位的正电荷。根据离子符号的书写特点(先写出元素的元素符号,然后再右上角标明该离子所带的电量及电性),所以钠离子的符号为Na 。
(2)①根据二者的溶解度曲线图可知:在t1℃时氯化钾的溶解度要大于硝酸钾的溶解度。
②根据图示可知:当温度由t2℃降温到t1℃时,硝酸钾的溶解度的变化值要选大于氯化钾的溶解度的变化值。所以当温度由t2℃降温到t1℃时,两物质的等质量的饱和溶液中,硝酸钾的溶液中析出的固体的质量大。
③根据图示可知,在t2℃时氯化钾的溶解度为40g。即在t2℃温度下,氯化钾在100g水里达到饱和状态时所溶解的质量为40g。因此题目中向100g水里50g氯化钾时,最多溶解40g加入溶剂。所以溶液为饱和溶液。 向溶液中再加入10g水,则水的总质量为110g,最多可溶解氯化钾的质量为44g,所以所得溶液仍为该温度下的氯化钾的饱和溶液。其溶质质量分数不变。
④欲配制溶质质量分数为20%的硝酸钾溶液,则要求硝酸钾的溶解度不小于25g。根据硝酸钾的溶解度曲线可知,温度范围为:温度不低于t1℃。
(3)氢氧化钠溶液呈碱性,可使酚酞变红。所以溶液原来为红色。随着加入的盐酸与氢氧化钠反应,溶液碱性逐渐减弱;当二者恰好完全反应时,溶液为中性,此时酚酞呈无色;再加入盐酸,则溶液呈酸性,溶液仍为无色。氢氧化钠与盐酸反应的化学方程式为:HCl NaOH==NaCl H2O 实验后测得试管中溶液的PH值为2,即溶液呈酸性。所以所含的溶质为氯化钠(为反应的生成物)、氯化氢(加入的过量的盐酸中的溶质)和原有的酚酞。
考点:元素周期表、原子的构成、溶解度曲线、化学方程式的书写、中和反应
23.(1)CaO;NH3;(2)3:1;正极;(3)CO CuO△ CuO CO2;(4)2H2 SiCl4△
Si 4HCl
【解析】
试题分析:A是水,通电时生成氢气甲和氧气乙,氢气和空气中含量最多的氮气在一定条件下反应生成氨气G,熟石灰F和硫酸铵在加热条件下反应能生成氨气; B是碳酸钙,在高温条件下分解生成二氧化碳C和氧化钙D,氧化钙和水反应生成氢氧化钙F;二氧化碳C和木炭丁在高温条件下反应生成一氧化碳E,氧气和铜戊在加热条件下反应生成氧化铜H,氧化铜和一氧化碳在加热条件下反应生成铜和二氧化碳;
氢气和四氯化硅在高温条件下发生置换反应生成硅单质和氯化氢气体,SiCl4 2H2高温Si 4HCl。
考点: 物质的鉴别、推断;书写化学方程式
24.①一定没有FeCl3和Na2SO4,一定有CaCO3、BaCl2、KOH,可能有KNO3;②BaCO3;③CaCO3 2HCl= CaCl2 CO2↑ H2O
【解析】
试题分析:无论是氢氧化铁沉淀,还是铁的盐溶液都是有颜色的,根据实验现象可以判断白色固体中一定不含有氯化铁;向白色沉淀中加入足量稀盐酸时,沉淀全部溶解,说明白色沉淀全部是碳酸钙,不含有硫酸钡,因为硫酸钡沉淀不溶于稀盐酸;向无色滤液中通入二氧化碳时,产生白色沉淀,是因为二氧化碳和氢氧化钾反应生成碳酸钾和水,碳酸钾和氯化钡反应生成了碳酸钡白色沉淀,因此白色固体中一定氢氧化钾和氯化钡,当含有氯化钡时,则一定不含有硫酸钠;硝酸钾是否存在,不影响上述实验现象的出现。①白色固体中一定不含有氯化铁和硫酸钠,一定含有碳酸钙、氯化钡和氢氧化钾,可能含有硝酸钾;②上述过程中通入CO2产生白色沉淀是碳酸钡,碳酸钡的化学式是BaCO3;③碳酸钙和稀盐酸反应的化学方程式为:CaCO3 2HCl═CaCl2 H2O CO2↑
考点:物质的鉴别、推断;碱的化学性质;盐的化学性质;书写化学方程式