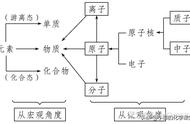
三、共价键
1、共价键的成键本质:
成键原子相互接近时,原子轨道发生重叠,自旋方向相反的未成对电子形成共用电子对,两原子核间电子云密度增加,体系能量降低。
2、共价键类型:
(1)σ键和π键

(2)极性键和非极性键

(3)配位键:一类特殊的共价键,一个原子提供空轨道,另一个原子提供一对电子所形成的共价键。
①配位化合物:金属离子与配位体之间通过配位键形成的化合物。如:Cu(H2O)4SO4、Cu(NH3)4(OH)2、Ag(NH3)2OH、Fe(SCN) 3等。
②配位化合物的组成:
3、共价键的三个键参数

(1)键长、键能决定共价键的强弱和分子的稳定性,键角决定分子空间构型和分子的极性。
(2)键能与反应热:反应热=生成物键能总和-反应物键能总和
四、分子的空间构型
1、等电子原理
原子总数相同、价电子总数相同的分子具有相似的化学键特征,许多性质是相似的,此原理称为等电子原理。
(1)等电子体的判断方法:在微粒的组成上,微粒所含原子数目相同;在微粒的构成上,微粒所含价电子数目相同;在微粒的结构上,微粒中原子的空间排列方式相同。(等电子的推断常用转换法,如CO2=CO O=N2 O=N2O=N2 N—=N3—或SO2=O O2=O3=N— O2= NO2—)
(2)等电子原理的应用:利用等电子体的性质相似,空间构型相同,可运用来预测分子空间的构型和性质。
2、价电子互斥理论
(1)价电子互斥理论的基本要点:ABn型分子(离子)中中心原子A周围的价电子对的几何构型,主要取决于价电子对数(n),价电子对尽量远离,使它们之间斥力最小。
(2)ABn型分子价层电子对的计算方法:
①对于主族元素,中心原子价电子数=最外层电子数,配位原子按提供的价电子数计算,如:PCl5中
②O、S作为配位原子时按不提供价电子计算,作中心原子时价电子数为6;
③离子的价电子对数计算
如:NH4 :;SO42- :
3、杂化轨道理论
(1)杂化轨道理论的基本要点:
①能量相近的原子轨道才能参与杂化。
②杂化后的轨道一头大,一头小,电子云密度大的一端与成键原子的原子轨道沿键轴方向重叠,形成σ键;由于杂化后原子轨道重叠更大,形成的共价键比原有原子轨道形成的共价键稳定。
③杂化轨道能量相同,成分相同,如:每个sp3杂化轨道占有1个s轨道、3个p轨道。
④杂化轨道总数等于参与杂化的原子轨道数目之和。
(2)s、p杂化轨道和简单分子几何构型的关系