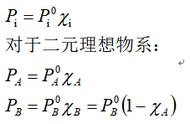(公式9) 3、热力学第三定律和标准摩尔熵 热力学第三定律 在绝对零度时,一切纯物质的完美晶体的熵值等于零。 物质的标准摩尔熵 规定熵(绝对熵):纯物质在温度T时的熵值。摩尔规定熵:1mol物质的规定熵,记作Sm(T)。标准摩尔熵:在标准状态下1mol物质的规定熵,记作Smθ(T)Ø 单位:J·K-1·mol-1Ø。 Smθ (稳定单质)≠0;S(0K)= 0 ;Smθ(H ,aq) = 0 熵值的大小规律 a. 同一物质,同温度:S(g) > S(l) > S(s) b. 同一物质,聚集状态相同:温度升高,熵值增大 c. 不同物质在温度相同、聚集状态相同:分子中微粒多者或组成复杂者熵值大 d. 化学反应熵值的定性判断:导致气体分子数增加的过程或反应熵值增大 标准摩尔反应熵的计算

(公式10) 近似处理:ΔrSmθ(TK)≈ΔrSmθ(298.15K) 4、吉布斯函数 定义:G = U PV-TS = H-TS G是状态函数;容量性质;单位J ;绝对值无法测知,无明确的物理意义 摩尔吉布斯函数:Gm= G/n;单位J·mol-1 △G的物理意义:等温等压下系统做非体积功的能力。 等温等压条件下的吉布斯函数判据 ΔG≤W 等温等压不做非体积功

等温过程ΔG的计算 ΔG = ΔH-T ·ΔS(公式11) ΔG = nRTln

=nRTln