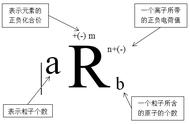
归纳整理
酸、碱、盐是初中化学中三种极其重要的物质,学习时必须从其宏观组成、微观构成、物质分类、溶液的导电性、溶液的酸碱性和酸碱度等方面做全面的分析和研究,为理解和掌握其化学性质和用途打下坚实的基础。
1.酸
(1)组成的共同点:酸中都含有氢元素和酸根,但学习中需要注意:①含有氢元素的化合物不一定是酸,如H2O,CH4以及盐

类物质中的NaHSO4等,它们虽然含有氢元素,但并不属于酸;②含有酸根的化合物也不一定是酸,如盐类物质。酸分子溶解于水时,能离解产生自由移动的H 和酸根离子,酸的水溶液能导电。要牢记:酸指的是溶于水时离解产生的阳离子全部是H 的化合物,这也正是酸类物质具有相似的化学性质的根本原因。
(2)酸的分类:根据酸的组成和性质可将酸分为:①含氧酸和无氧酸,如H2SO4、HNO3等属于含氧酸,HCl、H2S等属于无氧酸;②挥发性酸和不易挥发的酸,如HCl、HNO3等属于挥发性酸,H2SO4、H3PO4等属于不易挥发的酸;③稳定性酸和易分解的酸,如H2SO4、H3PO4等酸不易分解,H2CO3等酸易发生分解。
(3)酸溶液的pH:酸溶液的pH<7,且pH越小,酸性越强
(4)常见的酸:①盐酸—HCl;②硫酸—H2SO4;③硝酸—HNO3
2.碱
(1)组成的共同点:碱(除氨水)中都含有金属元素和氢氧根,但学习中需要注意:含有氢氧根这一原子团的化合物不一定是碱,如Cu2(OH)2CO3、Mg(OH)Cl等盐类物质,它们虽然含有氢氧根,但并不属于碱。碱溶于水时能离解产生自由移动的OH-和金属离子,碱的水溶液能导电。要牢记:碱指的是溶于水时离解产生的阴离子全部是OH—的化合物,碱的水溶液中都含有OH—离子,这正是碱类物质具有相似的化学性质的根本原因。。
(2)碱的分类:根据碱的溶解性可将其分为可溶性碱和难溶性碱,如NaOH、KOH等易溶于水,Ca(OH)2微溶于水,Cu(OH)2(蓝色)、Fe(OH)3(红褐色)等难溶于水。
(3)碱溶液的pH碱溶液的pH>7,且pH越大,碱性越强。
3.盐
(1)组成特点:由金属离子(或铵根离子)和酸根离子组成,但需要注意的是,盐溶解于水时离解产生的阳离子不一定全都是金属离子,而产生的阴离子也不一定全部是酸根离子。
(2)盐的分类:①根据含有相同金属离子进行分类:钠盐、钾盐、钙盐等;②根据含有相同的酸根离子;盐酸盐、硫酸盐、硝酸盐、碳酸盐等。
问题探究
问题1某食品防腐剂是一种酸的钠盐,其中各元素的质量分数为:C:58.33%,H:3.47%,O:22.2%,Na:16.0%。该物质的相对分子质量至少为 ( )A.144 B.72 C.36 D.54
[分析]盐中含有金属离子(或铵根离子)和酸根离子,若该钠盐的酸根用X表示且化合价为—n,则其化学式为NanX,其中n的最小值为1,根据此值可求出该盐的相对分子质量的最小值:23/16.0%==144
[答案]A
问题2酸、碱、盐三种化合物中:
(1)一定含有氢元素的是 、可能含有氢元素的是 ;
(2)一定含有氧元素的是 、可能含有氧元素的是 ;
(3) 可能含有两种元素、 一定不可能含有两种元素。
[分析]解决该问题可把有关概念作为思维的"原点",把"化抽象为具体"作为分析的一种方法。以问题(1)为例:根据酸和碱的概念发现其中无一例不含有氢元素;通过在熟悉的物质中寻找含有与不含有氢元素的盐,便可知道盐中是否一定含有氢元素。
[答案](1)酸和碱 盐 (2)碱 酸和盐 (3)酸和盐 碱
问题3混盐一般是由一种阳离子与两种酸根离子组成的盐,如:Ca(NO3)Cl。漂白粉中有一种混盐CaOCl2(其中钙元素化合价为 2,氧元素化合价为-2)。(1)请将该混盐改写成如Ca(NO3)Cl的形式,其化学式表示为 。(2)该混盐中氯元素的化合价为 。
[分析]CaOCl2中钙元素化合价为 2,氧元素化合价为—2,钙、氧两种元素的化合价的代数和为零,则其中氯元素定有正、负两种化合价且分别为 1、—1。依据Ca(NO3)Cl的化学式可知其中含有Ca2 、NO3—、Cl—,则CaOCl2中含有Ca2 、ClO—、Cl—。
[答案](1)Ca(ClO)Cl (2) 1、—1
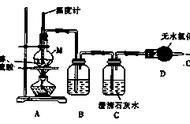
问题4氧化铜是一种黑色固体,可溶于稀硫酸:某同学想知道是稀硫酸中的哪种粒子(H2O、H 、SO42-)能使氧化铜溶解.请你和他一起通过下图I、II、III三个实验完成这次探究活动。(1)你提出的假设是 。

(2)通过实验I可以证明 。
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅲ中应该加入 。
(4)探究结果为 。你认为除实验Ⅱ和Ⅲ所用试剂外,还能够溶解氧化铜的一种常见物质是 。
[分析]此题应用对比实验确定稀硫酸中的哪种粒子(H2O、H 、SO42-)能使氧化铜溶解,对比实验就是控制变量实验。本实验涉及H2O、H 、SO42-三个变量,实验I通过控制H 、SO42-不出现,能得出H2O不能使氧化铜溶解的结论;由于II中同时出现了H2O、H 、SO42-三个变量,因此实验III中一定要控制H 不出现但SO42出现-或SO42-不出现而H 出现。
[答案](1)溶液中的H 使CuO溶解 (2)H20不能使CuO溶解 (3)盐酸(或硫酸钠溶液) (4)溶液中的H 可以使CuO溶解,H20、SO42-不能使CuO溶解
稀硝酸(或盐酸)
解后反思:
学以至用
一、选择题
1.酸和碱的组成中一定含有的元素是 ( )
A.氢元素 B.氧元素 C.氮元素 D.金属元素
2.有关酸、碱、盐、氧化物的说法不正确的是 ( )
A.酸和碱一定含有氢元素 B.盐和氧化物一定含有金属元素
C.碱和氧化物一定含有氧元素 D.酸和盐一定含有非金属元素
3.下列说法正确的是 ( )
A.酸、碱、盐中都含有原子团
B. 能使紫色的石蕊试液变蓝色的物质一定属于碱
C.盐溶解于水时离解生成的阳离子全部是金属离子
D.碱溶解于水时离解生成的阴离子全部是氢氧根离子
4.在a.单质、b.氧化物、c.酸、d.碱等四类物质中,经一步反应可以生成盐的是( )
A.只有abc B.只有cde C.只有abd D.abcd
5.将Ag的烧碱溶液与Bg的硫酸铜溶液充分混合,将反应所得的混合物过滤,得蓝色沉淀物和无色滤液。下列有关说法中正确的是 ( )
A.滤液中可能含有硫酸铜 B.滤液的pH一定等于7
C.滤液的质量一定小于(A B)g D.滤液中含有的溶质只可能为一种
6.某盐中所含有的元素>2种,其溶液中只含有一种溶质且阴、阳离子的个数比为1:2。
关于该盐的下列说法中,正确的是 ( )
A.可能含有NO3— B.一定不含有Cl—
C.一定含有金属元素 D.只含有三种元素
二、填空题
7.理性推测是化学研究的一种重要手段。A、B、C是中学化学中常见的化合物,其中C是正盐,已知:A nB =C H2O (方程式已配平),n为化学计量数。请回答下列问题:
(1)当n=1时,B是一种常见的酸,其相对分子质量是98,C的相对分子质量为120。则B的化学式为 ,A的相对分子质量为 ,经推测A的化学式为 。
(2)当n=2时,请各列举出一个化学反应方程式:
若A是一种酸性氧化物 ;若A是一种碱性氧化物 。
8.某课外兴趣小组,确立了"酸碱中和生成的正盐溶液的性质"作为研究课题,在研究中他们发现,正盐虽然不能电离出氢离子或氢氧根离子,但是其溶液却不一定呈中性,有的呈酸性,有的呈碱性。为什么呢?盐溶液的酸碱性与什么有关呢?由"组成、结构决定物质性质"的观点出发,他们又进一步从组成特征上去找原因, 发现正盐溶液的酸碱性与对应的酸和碱的强弱有关。他们将实验结果统计如下:

⑴请你根据上表归纳出正盐溶液的酸碱性与对应酸、碱的强弱关系:
。
⑵根据他们的发现,请你判断硝酸钠、硝酸铁、硫酸铜、氯化钾、磷酸钠、碳酸钾六种溶液的酸碱性,其中溶液呈酸性的是 、呈碱性的是 、呈中性的是 。
9.判断含氧酸(含有氧元素的酸)酸性强弱的一条经验规律是:含氧酸分子的结构中含非羟基(羟基为—OH)氧原子数越多,该含氧酸的酸性越强。

(1)根据以上信息可知,上表中X== 、Y== ;
(2)按照下列要求,请从不同的角度比较磷酸和硫酸:
①相同分子数时,物质的质量:磷酸 (填"大于"、"小于"或"等于")硫酸;
②溶液的质量及溶质的质量分数均相同时溶液的pH:磷酸溶液 (填"大于"、"小于"或"等于")硫酸溶液。
三、简答题
10.已知硫酸氢钠(NaHSO4)溶解于水时离解生成两种阳离子和硫酸根离子。请据此回答下列问题:
(1)离解生成的阳离子是哪两种?
(2)硫酸氢钠是不是酸?为什么?
11.小明学习了盐酸、硫酸后,知道它们的化学性质有许多相似之处。由此他联想通过实验探究食醋中的主要成分醋酸的化学性质(实验室能提供小明所需的各种仪器和药品)。请推测,他通过实验能得到有关醋酸化学性质的哪些结论?(至少说出三点)
四、实验探究题
12.某学生为证明浓盐酸具有挥发性和碳酸具有不稳定性,设计了如下实验:
(1)将石灰石和浓盐酸反应产生的气体通入紫色石蕊试液,来证明浓盐酸的挥发性。
(2)将上述已变红的石蕊试液加热煮沸.就可证明碳酸已分解。试分析实验设计的是否合理。并说明理由:
实验(1) 。
实验(2) 。
1.A 2.B 3.D 4.D 5.A 6.B
7.(1)H2SO4、40、MgO (2)CO2 2NaOH=Na2CO3 H2O(或SiO2、SO3、SO2等 2NaOH或KOH等)CuO 2HCl=CuCl2 H2O(或CaO、BaO、MgO等 2HCl或HNO3等);
8.⑴强酸和强碱生成的正盐溶液呈中性;强碱与弱酸生成的正盐溶液呈碱性;强酸与弱碱生成的正盐溶液呈酸性。⑵酸性:Fe(NO3)3、CuSO4;碱性:K2CO3、Na3PO4;中性:NaNO3、 KCl。
9.(1)1、2 (2)①等于 ②大于
10.(1)Na 、H (2)不是酸,因为碳酸氢钠溶于水时离解产生的阳离子不全都是氢离子
11.(1)能使紫色的石蕊试液变红,不能使无色的酚酞试液变色;(2)能和某些金属单质发生置换反应;(3)能和某些金属氧化物反应;(5)能和碱反应,生成盐和水;(5)能和碳酸盐反应,生成二氧化碳气体。
12.(1)不合理,因为CO2 通人紫色石蕊故液,试液也能变红,故不能直接验证浓盐酸的挥发性。(2)不合理,因为加热煮沸不能除尽氯化氢.故不能直接验证碳酸的不稳定性。
提示;对化学实验的现象分析要关注有没有干扰因素的存在。
,