1,根据反应中物质得氧或失去氧,把化学反应分为氧化反应和还原反应。得氧的反应是氧化反应,失氧的反应是还原反应。
2,从化合价升降的角度分析氧化还原反应
物质所含元素化合价升高的反应是氧化反应,物质所含元素化合价降低的反应是还原反应。凡是元素化合价产生升降变化的反应就是氧化还原反应。
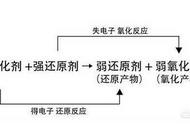
3,从电子得失的角度分析氧化还原反应
物质失去电子的反应是氧化反应,物质得到电子的反应是还原反应。凡是产生电子得失的反应就是氧化还原反应。
所以,反应前后有元素的化合价发生变化,是氧化还原反应的重要特征。氧化还原反应的本质:存在电子转移。有的是电子得失,有的是共用电子对偏移。
氧化反应表现为:元素的原子失去电子(或电子对偏移),则元素的化合价升高,物质被氧化;
还原反应表现为:元素的原子得到电子(或电子对偏向),则元素的化合价降低,物质被还原。



,