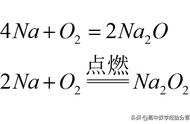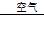第2课时 氧化钠和过氧化钠
学习目标
1.从物质类别、元素化合价的角度认识氧化钠与过氧化钠的性质,熟知过氧化钠与水和二氧化碳反应的应用。
2.会设计实验探究过氧化钠与水的反应,增强科学探究与创新意识。
重难点
1.过氧化钠与水、与CO2反应的化学方程式。
2.形成结构决定性质,性质决定用途的观念,初步构建“宏观辨识与微观探析”的学科核心素养。
知识导学
一、氧化钠和过氧化钠的性质
1.物理性质
氧化钠是一种 固体,过氧化钠是一种 固体。
注意 Na2O2中阴、阳离子数之比是 而不是1∶1。
2.氧化钠的化学性质
氧化钠是碱性氧化物,写出下列反应的化学方程式:
(1)氧化钠与水反应: 。
(2)氧化钠与盐酸反应: 。
(3)氧化钠与二氧化碳反应: 。
3.过氧化钠的化学性质
(1)实验探究过氧化钠与水的反应
实验操作 | |
实验现象 | ①试管外壁 ,带火星的木条 ;②用pH试纸检验反应所得溶液呈 性 |
实验结论 | Na2O2与水反应 ,化学方程式为 。 |
(2)过氧化钠与二氧化碳反应的化学方程式: 。
二、过氧化钠与水、二氧化碳反应的定量关系
1.化学方程式
____________________________________;___________________________________。
回答下列问题。
(1)Na2O2中氧的化合价为-1,在两个反应中Na2O2的作用是________________(填“氧化剂”“还原剂”或“既做氧化剂又做还原剂”),从电子转移角度分析,每生成一分子氧气转移____个电子。每消耗一个Na2O2转移______个电子。
(2)从化学方程式的计量数分析可知,无论是CO2、H2O还是二者的混合物,通过足量的Na2O2时,CO2或H2O与放出O2的分子个数之比均为_________。
2.Na2O2与CO2、H2O反应的质量关系
(1)2Na2O2+2CO2===2Na2CO3+O2 Δm(固体)
2×78 2×44 2×106 56
即发生反应时,固体增加的质量等于与CO2等分子数的CO的质量。
(2)2Na2O2+2H2O===4NaOH+O2↑ Δm(固体)
2×78 2×18 4×40 4
即发生反应时,固体增加的质量等于与H2O等分子数的H2的质量。
1.(2020·巩义市第四高级中学月考)下列关于Na2O与Na2O2的说法中,错误的是( )
A.两者颜色不同
B.均可与H2O、CO2反应
C.Na2O能被氧化成Na2O2
D.它们的固体溶于水滴加酚酞试液后,现象相同
2.(2020·湖南天心·长郡中学高二开学考试)在溶液中加入适量Na2O2后仍能大量共存的是( )
A.NH4+、Ba2 、C1-、NO3- B.Na 、Mg2 、C1-、C1O-
C.Cu2 、Na 、NO3-、HCO3- D.K 、AlO2-、C1-、SO42-
3.(2021·河北易县中学高二月考)取10.8g平均相对分子质量为7.2的CO与H2组成的混合气体,与足量的O2充分反应后,立即将产物通入足量的Na2O2固体中,反应后Na2O2固体质量增加为( )
A.3.6g B.7.2g C.10.8g D.无法确定
4.(2020·辽宁六校高一期中)某同学结合所学知识探究Na2O2与H2能否反应,设计装置如下,下列说法正确的是( )
A.若D中无水硫酸铜变蓝,则说明Na2O2与H2反应生成水
B.装置B中盛放浓硫酸,目的是除去A中挥发出来的少量水蒸气
C.装置C加热前,用试管在干燥管管口处收集气体点燃,通过声音判断气体纯度
D.装置A不能直接用于H2O2与MnO2反应制取氧气
,