第六单元 课题2
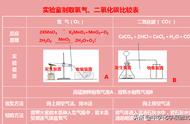
二氧化碳制取的研究
一.药品的选择
实验室制备气体时选择药品应满足:
(1) 药品廉价,易得;
⑵ 反应速率适中,反应能够持续一段时间;
⑶ 反应物中无气体,只生成一种气体;
(4) 符合环保意识,尽量不浪费能源
1、根据以上原则,以下四种方法哪种最适合用于实验室制取二氧化碳? ;
A. C O2 点燃 CO2
B. 2CuO C 高温 2Cu CO2↑
C. CaCO3 高温 CaO CO2↑
D. CaCO3+2HCl=CaCl2+H2O+CO2↑
分析:
A项中反应物中有气体,不利于收集到纯净的气体。
B项中反应条件是高温,不利于到达反应条件,
C项中条件是高温,不利于到达实验条件。
D项中,CaCO3碳酸钙在自然界中很常见,大理石的主要成分就是它,稀盐酸在实验室也很常用。且只生成一种气体。
2根据以上原则,实验室制取二氧化碳所用的药品,有如下四种中都能产生二氧化碳,哪种更合理?
A.块状的石灰石和浓盐酸;
B.块状的石灰石和稀盐酸;
C.块状的石灰石和稀硫酸;
D.碳酸钙粉末和稀盐酸;
解析:
A中浓盐酸具有挥发性,会导致收集到的气体不纯净;且浓盐酸浓度大,导致反应速率过快。
C项中,大理石和稀硫酸反应,因为生成了微溶于水的硫酸钙,会阻止反应逐渐停止。
D项中,由于粉末和稀盐酸接触面积过大,导致反应速率过快,不利于收集。
B项反应速率适中。可选。
二:装置的选择
确定好药品后,进行装置的选择。
1、在实验室制取气体实验中

(1)①如果反应物的状态是 固体 ,反应条件 加热 ,选用发生装置 A ; (填序号)
②如果反应物的状态是 液体 ,反应条件 不需加热 ,选用发生装置 B或C ;
所以,选择发生装置的选择依据: 1、药品的状态2、反应条件是否需要加热 。
(2)收集装置的选择依据:主要是气体的物理性质等,包括气体的密度和溶解性。
①排水法:适用于收集 难溶于水的气体 ,且不能与水反应
②向上排空气法:适用于收集 密度比空气大的气体 ,且不与空气中物质反应 。
③向下排空气法:适用于收集密度比空气小的气体 ,且不与空气中物质反应。
所以,选择收集装置的选择依据: 溶解性、密度与空气的比较 。
2、根据选择的药品为:块状大理石和稀盐酸,且反应不需要加热。
那么制取二氧化碳所选用的发生装置的类型是: 固液不加热 型(上图B或C)
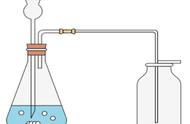
根据以前制取气体的相关知识,根据以下具体要求设计制取二氧化碳的实验装置。请用以下仪器(且不限于以下仪器)设计相应的实验装置图。【提示:发生装置和收集装置最好分开】
1、甲同学 想用最少的仪器,最简易的装置制、取二氧化碳,该如何设计?

2、乙同学 想在反应过程中不断添加液体药品,该怎么设计实验“发生”装置?

3、丙同学 想精确控制液体药品用量,可怎么设计“发生装置”?

4、丁同学 想安装一个可以控制,随时开始,随时停止的反应装置,该如何设计“发生装置”?

三、实验室制取二氧化碳的步骤

第一步:检查装置气密性。(将橡胶管夹紧,向长颈漏斗中加入一定量的液体,待液体没过长颈漏斗下端后,若漏斗中液面保持不变,则气密性良好)
第二步:加固体药品。
第三步:加液体药品。
第四步:收集气体。
(视频:观看视频,注意操作技巧和复习知识)
注:1、验满方法:将“燃着”的木条放置在瓶口,若熄灭则已满。
2、检验是否为二氧化碳的方法:加入澄清石灰水,震荡,若变浑浊,则为二氧化碳。
原理:Ca(OH)2 CO2=CaCO3↓ H2O
欢迎关注微信公众号 :中学高分宝典
,