考题训练(十三)__物质的溶解性
夯 实 基 础
1.已知 20 ℃时,氯化钠的溶解度为 36 g。此时,20 g 水中最多能溶解氯化钠的质量为( )
A.36 g B.3.6 g C.7.2 g D.10 g
2.现有一杯 20 ℃的硝酸钾不饱和溶液,能改变硝酸钾溶解度的操作是( )
A.加硝酸钾 B.充分搅拌
C.恒温蒸发水 D.升高温度
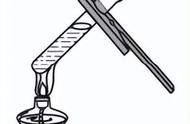
3.在粗盐的初步提纯实验中,下列操作正确的是( )
图 K13-1

4.【2016·龙东】在粗盐提纯的实验操作中,下列说法正确的是( )
A.过滤时用到的仪器:烧杯、玻璃棒、铁架台、滤纸
B.蒸发操作结束后,将蒸发皿放在石棉网上
C.用药匙将蒸发皿中的白色固体直接转移到纸上
D.实验结束后所得到的白色固体为氯化钠
5.硝酸钾在不同温度下的溶解度数据如下表。下列说法错误的是( )
温度/℃ 0 20 40 60 80 100
溶解度/g 13.3 31.6 63.9 110 169 246
A.硝酸钾的溶解度受温度的影响较大
B.60 ℃时,饱和硝酸钾溶液中溶质与溶液的质量之比为 11∶21
C.20 ℃时,10 g 水中加入 5 g 硝酸钾充分溶解后再加入 5 g 水,前后溶质的质量分数不变
D.将溶质质量分数为 28%的硝酸钾溶液从 60 ℃降温至 20 ℃,没有晶体析出
6.
图 K13-2

【2016·北京】甲、乙的溶解度曲线如图 K13-2 所示。下列有关说法不正确的是( )
A.t2℃时,甲的饱和溶液中溶质和溶剂的质量之比为 2∶5
B.t2℃时,乙的饱和溶液降温到 t1℃后,溶液仍饱和
C.t1℃时,甲、乙两种饱和溶液中溶质的质量相等
D.甲、乙的饱和溶液分别从 t2℃降温到 t1℃,两溶液中溶质质量分数相等
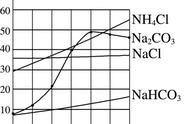
7.某盐化工厂生产的碳酸钠粗产品中含有少量的氯化钠。碳酸钠和氯化钠的溶解度与温度的关系如图 K13-3 所
示,请回答:
图 K13-3

(1)t1℃时碳酸钠与氯化钠中溶解度较大的物质是____________________。
(2)t1℃时碳酸钠溶液升温至 t2℃,所得溶液的溶质质量分数________(填"变大""变小"或"不变")。
(3)除去碳酸钠中混有的少量氯化钠的方法是________________。
8.【2016·南宁】根据下表中氯化钠和硝酸钾部分溶解度数据分析回答下列问题。
温度/℃ 0 10 20 30 40 50 60
溶解
度/gNaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110
(1)10 ℃时,氯化钠的溶解度是________g。
(2)硝酸钾的溶解度随温度的升高而________;与硝酸钾相比较,氯化钠的溶解度受温度变化影响________(填"较
大"或"较小")。
(3)20 ℃时,在 100 g 水中加入 40 g 硝酸钾,充分搅拌后,将溶液温度升高到 30 ℃(不考虑水分蒸发),所得溶
液是________________(填"饱和溶液"或"不饱和溶液")。
(4)在 20~30 ℃的某温度时,氯化钠和硝酸钾的溶解度(x)相同,x的取值范围是______________。
能 力 提 升
1.【2017·邵阳】在"粗盐难溶性杂质的去除"实验中,操作步骤为溶解、过滤、蒸发、计算产率。下列各步骤
中的一些做法正确的是( )
A.溶解:用玻璃棒搅拌以加速溶解
B.过滤:直接将粗盐水倒入漏斗中
C.蒸发:等蒸发皿中水分蒸干便停止加热
D.计算产率:将精盐直接转移到天平的托盘上称量
2.【2017·济宁】酸、碱、盐的溶解性表为我们确定常见物质的溶解性提供了方便,下表是溶解性表中的一部分,
结合表格和溶解度知识判断,下列说法不正确的是( )
常见酸、碱、盐的溶解性表(20 ℃)
OH- NO3- Cl- SO4
2- CO32-
Ca2+
微 溶 溶 微 不
A.绘制表格的依据是物质的溶解度
B.常见物质一般可分为:溶、微溶和不溶
C.Ca(OH)2、CaSO4和 CaCO3的溶解度都大于 1 g
D.Ca2+、NO3
-、Cl
-三种离子在溶液中能大量共存
3.【2017·本溪】甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图 K13-4 所示,请回答下列问题。
图 K13-4