【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水
剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是 Mg3N2。
【实验探究】请设计实验,验证猜想
实验操作 实验现象及结论
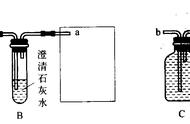
__收集产物中的黄色固体放入试管中,加入
适量的水,在试管口放置湿润的红色石蕊试
纸__
__有刺激性气味的气体生成,试纸由红色变
蓝色;黄色固体是 Mg3N2__
【反思与交流】
①氮化镁中氮元素的化合价是__-3__价。
②空气中 N2的含量远大于 O2的含量,可是镁条在空气中燃烧的产物 MgO 却远多于 Mg3N2,合理的解释是:__氮
气的化学性质不如氧气活泼__。
③同学们又联想到氢气在氯气中能够燃烧,于是对燃烧条件又有了新的认识:__燃烧不一定需要有氧气参加
__。
16.200 g 某硫酸恰好与 26 g 锌完全反应,试计算:
(1)生成氢气的质量。
(2)硫酸溶液中溶质的质量分数。
(3)充分反应后所得溶液的质量。
解:(1)设生成氢气的质量为 x,硫酸中溶质的质量为 y。
Zn+H2SO4===ZnSO4+H2↑
65 98 2
26 g y x
65
26 g=98
y=2
x
x=0.8 g y=39.2 g;
(2)硫酸溶液中溶质的质量分数为:39.2 g
200 g×100%=19.6%;
"
(3)充分反应后所得溶液的质量为:
200 g+26 g-0.8 g=225.2 g。
答:(1)生成氢气的质量为 0.8 g;(2)硫酸溶液中溶质的质量分数为 19.6%;(3)充分反应后所得溶液的质量
为 225.2 g。