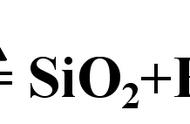U是中子数不同质子数相同的同种核素
D. 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构
考点:核素;元素周期表的结构及其应用;化学键;芳香烃、烃基和同系物.
专题:原子组成与结构专题;元素周期律与元素周期表专题;化学键与晶体结构;有机化学基础.
分析:A.结构相似,分子组成上相差1个或者若干个CH2基团的化合物互称为同系物;
B.同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性共价键;
C.核素是指具有一定数目质子和一定数目中子的一种原子;
D..ⅣA(用X表示)与ⅦA(用Y表示)形成的化合物为XY4.
解答:解:A.乙酸含有一个羧基,丙二酸含有2个羧基,结构不相似,不互为同系物,故A错误;
B.如 H2O2分子,分子中含有一个O﹣O非极性键,故B错误;
C.

U和

U的中子数不同,不是相同的同种核素,故C错误;
D.ⅣA(用X表示)与ⅦA(用Y表示)形成的化合物为XY4,X形成四个键,加上原来的4个电子,最外层共8个电子,每个Y形成一个键,加上原来的7个电子,共8个电子,故D正确.
故选D.
点评:本题考查同系物、极性键、核素等,题目难度不大,注意知识的积累.
二.填空题(共1小题)
8.(2012•上海)2009年《自然》杂志报道了我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定"北京人"年龄的研究结果,这种测量方法叫"铝铍测年法".完成下列填空:
(1)10Be和9Be cd .
a.是同一种原子 b.具有相同的中子数
c.具有相同的化学性质 d.具有恒定的丰度
(2)Be所在的周期中,最外层有2个未成对电子的元素相互组成的化合物属于 分子 晶体.
(3)Al和Be具有相似的化学性质,写出BeCl2水解反应的化学方程式 BeCl2 2H2O⇌Be(OH)2 2HCl .
(4)研究表明26Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是 BC .
A.比较这两种元素的单质的硬度和熔点
B.在氯化铝和氯化镁的溶液中分别滴加过量的氢氧化钠溶液
C.将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液
D.将空气中放置已久的这两种元素的单质分别和热水作用
(5)目前还有一种测量方法叫"钾氩测年法".写出和Ar核外电子排布相同的阴离子的半径由大到小的顺序 S2﹣>Cl﹣ (用化学符号表示);其中一种离子与钾相邻元素的离子所形成的化合物可用做干燥剂,此化合物的电子式是

.
考点:同位素及其应用;元素周期律和元素周期表的综合应用.
分析:(1)10Be和9Be的质子数相同、中子数不同,属于同位素;
(2)Be所在的周期中,最外层有2个未成对电子的元素分别为C、O,二者相互组成的化合物有CO、CO2,根据物质的构成微粒确定晶体类型;
(3)Al和Be具有相似的化学性质,根据AlCl3水解反应知,BeCl2水解生成Be(OH)2和HCl;
(4)金属的金属性强弱的比较方法有:金属之间的置换反应、金属与同种酸或水生成氢气的难易程度、金属的最高价氧化物的水化物碱性强弱等来判断;
(5)和Ar核外电子排布相同的阴离子有S2﹣、Cl﹣,电子层结构相同的离子,其离子半径随着原子序数的增大而减小;其中一种离子与钾相邻元素的离子所形成的化合物可用做干燥剂,该干燥剂是CaCl2,CaCl2中阴阳离子之间存在离子键.
解答:解:(1)10Be和9Be的质子数相同、中子数不同,属于同位素,
a.其质量数不同,所以不是同一种原子,故错误;
b.10Be和9Be的中子数分别为6、5,所以其中子数不同,故错误;
c.决定化学性质的是其最外层电子,二者的核外电子排布相同,所以同位素具有相同的化学性质,故正确;
d.同位素具有恒定的丰度,故正确;
故选cd;
(2)Be所在的周期中,最外层有2个未成对电子的元素分别为C、O,二者相互组成的化合物有CO、CO2,CO、CO2晶体的构成微粒都是分子,所以都属于分子晶体,
故答案为:分子;
(3)Al和Be具有相似的化学性质,根据AlCl3水解反应知,BeCl2水解生成Be(OH)2和HCl,氯化铍的水解方程式为BeCl2 2H2O⇌Be(OH)2 2HCl,
故答案为:BeCl2 2H2O⇌Be(OH)2 2HCl;
(4)A.金属性强弱与其单质的硬度和熔点无关,故错误;
B.在氯化铝和氯化镁的溶液中分别滴加过量的氢氧化钠溶液,氢氧化铝能溶于NaOH溶液,而氢氧化镁不溶于NaOH溶液,所以Mg的金属性大于Al,故正确;
C.将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液,Mg和沸水的溶液呈红色、Al和沸水的溶液不变色,说明Mg能置换出氢气,则Mg的活泼性大于Al,故正确;
D.将空气中放置已久的这两种元素的单质分别和热水作用,二者表面都生成氧化物薄膜,氧化镁和氧化铝都不与水反应,所以无法判断金属性强弱,故错误;
故选BC;
(5)和Ar核外电子排布相同的阴离子有S2﹣、Cl﹣,电子层结构相同的离子,其离子半径随着原子序数的增大而减小,所以这两种离子半径大小顺序是S2﹣>Cl﹣;其中一种离子与钾相邻元素的离子所形成的化合物可用做干燥剂,该离子是钙离子,该干燥剂是CaCl2,CaCl2中阴阳离子之间存在离子键,其电子式为