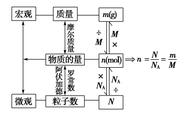
摩尔质量—克/摩
单位物质的量的物质所具有的质量,即1摩尔物质的质量。实际上就是1 mol 该物质分子的质量。从这个定义就知道,质量与摩尔质量是不一样的,
他们的单位也不一样。摩尔质量数值上等于相对原子质量或者相对分子质量。
举例:
1mol氧气的质量是32g,那么氧气的摩尔质量就是32g/mol。氧气的相对分子质量是32。
1mol 质量是23g,那么钠的摩尔质量就是23g/mol。钠的相对原子质量是23。
那么:
32g氧气就是1mol;
64g氧气就是mol;
mg氧气就是mol;
mg就是mol;
于是我们可以得到一个公式:
n=m/M
其中M是摩尔质量

气体摩尔体积—升/摩
标准状况下,单位物质的量的气体所占有的体积为22.4L,即1摩尔
气体的体积。实际上就是气体分子占有的体积约为 22.4L。
和摩尔质量一样的推导法,我们得到一个公式:Vm=V/n
物质的量浓度—摩/升
在一定温度和压强下,单位体积中所含溶质物质的量的多少,即1L溶液中含有溶质的物质的量,实际就是1L溶液中含有多少个个溶质分子。
公式:C=V/n
在这些概念中,最本源的是什么,其实就是阿佛加德罗常数NA和摩尔。其他的概念和定义都建立在它们的基础上。