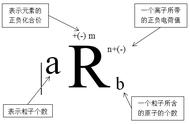
注意:元素的化学性质由最外层电子数决定
二、离子
1.离子:带电的原子(或原子团)叫离子。
2.分类
阳离子:带正电的原子或原子团。如:钠离子(Na )、镁离子(Mg2 )、铵根离子
阴离子:带负电的原子或原子团。如:氯离子(Cl-)、硫离子(S2-)、硫酸根离子()。
注意:阴、阳离子由于静电作用互相吸引,结合形成稳定的、不带电性的化合物。
3.离子的形成过程
(1)金属原子的最外层电子数一般小于4个,在化学反应中易失去电子,质子数大于核外电子数,所以带正电荷,为阳离子,电子层减少1层。
(2)非金属原子的最外层电子数一般多于4个,在化学反应中易得到电子,质子数小于核外电子数,所以带负电荷,为阴离子,电子层数不变。
2.离子符号
(1)离子符号表示的意义
离子用离子符号表示:在原子团或元素符号的右上角标出离子所带的电荷的多少及电荷的正负(数字在前,符号在后),当离子所带电荷数为1时,1可以不写。如Na (钠离子)、Ca2 (钙离子)、H (氢离子)、Cl-(氯离子)、O2-(氧离子)、OH-(氢氧根离子)等。
离子符号表示的意义:Mg2 表示1个镁离子带2个单位的负电荷。2O2-表示2个氧离子。
离子符号只有微观含义,没有宏观含义。

(2)分子、原子和离子的区别和联系

三、相对原子质量
1.定义
以一种碳原子(碳12原子)的质量的1/12为标准,其他原子的质量与这个标准的比值,就是该原子的相对原子质量。
2.公式
某种原子的相对原子质量(Ar)=

3.理解相对原子质量的几个注意事项
(1)相对原子质量是一个比值,不是原子的实际质量。
(2)相对原子质量有单位,国际单位为“1”,一般不写。
(3)作为标准的是碳12原子实际质量的1/12,而不是碳原子的质量。
4.原子的质量与相对原子质量的区别和联系