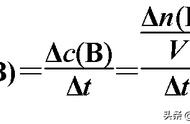学习目标
1.变化观念:了解化学反应速率的概念及其表示方法,形成不同的反应可用不同的方法来表 示化学反应速率的变化观念。
2.证据推理:根据化学反应速率的测定原理设计实验,学会化学反应速率的测定方法
3.从宏观上认识外界因素影响化学反应速率的规律,并能从活化分子的有效碰撞等微观的角 度进行分析解释
知识导学
知识点 1 化学反应速率及其测定
1.化学反应速率的概念及其表示方法

2.化学反应速率的测定
(1)测定原理 利用与化学反应中任何一种化学物质的浓度相关的可观测量进行测定。
(2)测定方法
①直接观察测定:如释放出气体的体积和体系的压强等。
②科学仪器测定:如反应体系颜色的变化。在溶液中,当反应物或生成物本身有较明显的颜 色时,可利用颜色变化和显色物质与浓度变化间的比例关系来跟踪反应的过程和测量反应速 率。
例 1.在反应 N2+3H2 2NH3中,经过一段时间后,NH3的浓度增加了 0.6 mol·L -1,在此 段时间内用 H2表示的平均反应速率为 0.45 mol·L -1·s-1,则此段时间是( )
A.1 s B.2 s C.44 s D.1.33
例 2.已知 4NH3(g)+5O2(g)===4NO(g)+6H2O(g),若化学反应速率分别用 v(NH3)、v(O2)、 v(NO)、v(H2O)(单位:mol·L -1·s-1)表示,则下列关系正确的是( )

归纳总结

知识点 2 化学反应速率的计算和比较
1.化学反应速率的计算
(1)公式法: