一、原子结构发展史认识。
二、描述原子核外运动状态。
能层、能级、原子轨道与电子自旋
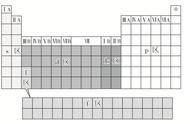
三、原子结构与元素周期表。
横行7个周期,纵行16个族ⅠA~Ⅷ ⅠB~ⅦA 0(ⅡA族之后ⅢB,ⅡB之后ⅢA)
周期序数=原子最大能层数
主族序数=原子最外层电子数=原子价电子数(ⅠA、ⅡA属S区ⅢA~ⅦA属P区)
ⅢB~ⅦB族序数=原子价电子数
Ⅷ族价电子数之和为8、9、10
ⅢB~ⅦB、Ⅷ属d区
ⅠB(价电子数11)、ⅡB(价电子数12)属dS区
0族最外层电子数8(He最外层电子数2)属P区
四、原子核外电子排布遵循几个原则。
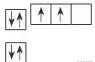
能量最低原理(电子填充原理)、泡利原理(一个原子轨道内电子填充)、洪特规则(能量相同轨道电子填充)。
五、原子及核外电子表达。
原子结构示意图 电子式 核外电子排布式
价电子排布式 简化电子排布式
核外电子排布图(轨道表示式)价电子排布图
第三能层(某能层)电子排布式
六、基态与激发态、原子光谱。
基态与激发态原子认识,吸收光谱与发射光谱认识及光谱分析。